
 Cu(HDz)2+2H+,ŌŁ¼ÓČėCCl4,Cu(HDz)2¾ĶŗÜČŻŅ×±»ŻĶČ”µ½CCl4ÖŠ”£
Cu(HDz)2+2H+,ŌŁ¼ÓČėCCl4,Cu(HDz)2¾ĶŗÜČŻŅ×±»ŻĶČ”µ½CCl4ÖŠ”£
 )±ŲŠė×Ŗ»»³É¹ÆĄė×Ó(Hg2+)²ÅÄÜÓĆĖ«ĮņėźĀēŗĻ”£Ä³¹¤³§ĪŪĖ®ÖŠŗ¬ÓŠ½Ļ¶ąµÄĀČ»ÆŃĒ¹Æ(Hg2Cl2),¼ÓČė¶žĮņĖį¼Ų(K2S2O8)æÉŃõ»ÆH
)±ŲŠė×Ŗ»»³É¹ÆĄė×Ó(Hg2+)²ÅÄÜÓĆĖ«ĮņėźĀēŗĻ”£Ä³¹¤³§ĪŪĖ®ÖŠŗ¬ÓŠ½Ļ¶ąµÄĀČ»ÆŃĒ¹Æ(Hg2Cl2),¼ÓČė¶žĮņĖį¼Ų(K2S2O8)æÉŃõ»ÆH Éś³ÉĮņĖį¹Æ,Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½:”””£
Éś³ÉĮņĖį¹Æ,Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½:”””£ 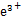 +3H2Dz
+3H2Dz Fe(HDz)3+3H+””Fe3+»įŠĪ³ÉFe(OH)3³Įµķ
Fe(HDz)3+3H+””Fe3+»įŠĪ³ÉFe(OH)3³Įµķ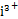 ”ĆBi(HDz)3=3”Ć2
”ĆBi(HDz)3=3”Ć2 Zn(OH
Zn(OH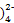 +2Dz2-+2H2O
+2Dz2-+2H2O 2HgSO4+2KCl
2HgSO4+2KCl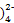 ,H2DzŹōÓŚ¶žŌŖČõĖį,×īÖÕŅŌDz2-ŠĪŹ½“ęŌŚ
,H2DzŹōÓŚ¶žŌŖČõĖį,×īÖÕŅŌDz2-ŠĪŹ½“ęŌŚ

 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĒāŃõ»Æ±µÓėĻ”ĮņĖį·“Ó¦£ŗBa2£«£«SO42£=BaSO4”ż |
| B£®Al2O3ČÜÓŚŃĪĖįÖŠ£ŗO2£+2H+=H2O |
| C£®ĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČėÉŁĮæ°±Ė®£ŗAl3+ + 3OH£= Al(OH)3”ż |
D£®ĀČĘųÓėĖ®·“Ó¦ Cl2+H2O H+ + Cl£+ HClO H+ + Cl£+ HClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÓĆĢ¼ĖįÄĘČÜŅŗ“¦ĄķĖ®¹øÖŠµÄĮņĖįøĘ£ŗCa2£«£«CO32”Ŗ=CaCO3”ż |
| B£®ĮņĖįŠĶĖįÓź·ÅÖĆŅ»¶ĪŹ±¼äČÜŅŗµÄpHĻĀ½µ£ŗ2H2SO3£«O2=2H2SO4 |
| C£®Ļņ¹čĖįÄĘČÜŅŗÖŠµĪČėĻ”ŃĪĖįµĆµ½½ŗĢå£ŗNa2SiO3£«2HCl=H2SiO3(½ŗĢå)£«2NaCl |
| D£®ÓĆŹÆÄ«µē¼«µē½āAlCl3ČÜŅŗŅõ¼«ø½½üÉś³É³Įµķ£ŗ2Al3£«£«6H2O£«6e£=2Al(OH)3”ż£«3H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÄÜĖµĆ÷Ńõ»ÆŠŌH2O2>Fe3£«£ŗ2Fe2£«£«H2O2£«2H£«=2Fe3£«£«2H2O |
| B£®ÄÜĖµĆ÷NH3½įŗĻH£«ÄÜĮ¦±ČH2OĒæ£ŗNH3£«H3O£«=NH4+£«H2O |
| C£®ÄÜĖµĆ÷ŃĪĖįŹĒĒæĖį£ŗ2HCl£«CaCO3=CaCl2£«CO2”ü£«H2O |
D£®ÄÜĖµĆ÷CH3COOHŹĒČõµē½āÖŹ£ŗCH3COO££«H2O CH3COOH£«OH£ CH3COOH£«OH£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĒāŃõ»ÆĆ¾ÓėĻ”ŃĪĖį·“Ó¦£ŗH£«£«OH£===H2O |
| B£®AlCl3ČÜŅŗÖŠ¼ÓČėÉŁĮæ°±Ė®£ŗAl3£«£«3OH£===Al(OH)3”ż |
| C£®ĶČÜÓŚĻ”ĻõĖį£ŗ3Cu£«8H£«£«2NO3”Ŗ===3Cu2£«£«2NO”ü£«4H2O |
| D£®“ĪĀČĖįøĘČÜŅŗÖŠĶØČė¹żĮæCO2£ŗCa2£«£«2ClO££«H2O£«CO2===CaCO3”ż£«2HClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®½šŹōÄĘĶ¶ČėÕōĮóĖ®2 Na+2H2O£½2 Na++2OH- +H2”ü |
| B£®ĻņŃĒĮņĖįÄĘČÜŅŗÖŠ¼ÓČė×ćĮæĻõĖįSO3 2- +2 H+=SO2”ü+ H2O |
| C£®ÓĆÅØŃĪĖįÓėMnO2·“Ó¦ÖĘȔɣĮæĀČĘųMnO2+4H++2C1- = Mn2+ + 2H2O+Cl2”ü |
| D£®ĮņĖįŃĒĢśČÜŅŗÖŠ¼ÓČėĖį»ÆµÄĖ«ŃõĖ®Fe2++2H++H2O2 = Fe3++2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®CO+CuO Cu+CO2 Cu+CO2 |
| B£®2Na+2H2O=2NaOH+H2”ü |
| C£®Fe+CuSO4=FeSO4+Cu |
| D£®2FeCl3+Cu=2FeCl2+CuCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ČŪČŚµÄNaHSO4µēĄėNaHSO4£½Na + + H + + SO2©¤ 4 |
B£®HCO©¤ 3ŌŚĖ®ČÜŅŗÖŠĖ®½ā£ŗ HCO©¤ 3£«H2O H3O+ + CO2©¤ 3 H3O+ + CO2©¤ 3 |
| C£®AlCl3ČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė®µÄ·“Ó¦£ŗ Al3+ + 4OHŅ»£½ A1O©¤ 2£« 2H2O |
| D£®µē½āNa2SO4ČÜŅŗµÄŅõ¼«·“Ó¦£ŗ 2 H2O + 2eŅ»£½ 2OHŅ»£« H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®½«4 molCl2ĶØČėµ½ŗ¬ÓŠ4 mol FeBr2µÄČÜŅŗÖŠ£ŗ2Cl2£«2Fe2+£«2Br££½ 4Cl££«Br2£«2Fe3+ |
| B£®ŅŃÖŖŃĒĮņĖį£ØH2SO3£©µÄµŚ¶ž¼¶µēĄė³£ŹżK2±ČĘ«ĀĮĖį£ØHAlO2£©µÄµēĄė³£ŹżKŅŖ“ó£¬Ōņ½«ÉŁĮæµÄSO2ĘųĢåĶØČėµ½Ę«ĀĮĖįÄĘČÜŅŗÖŠ·¢ÉśµÄĄė×Ó·“Ó¦ŹĒ£ŗAlO2££« SO2£«2 H2O £½Al(OH)3”ż£«HSO3£ |
| C£®Ļ”°±Ė®ČÜŅŗĪüŹÕĮĖÉŁĮ涞Ńõ»ÆĢ¼ĘųĢå£ŗ NH3 ”¤H2O £« CO2 £½ NH4+ £« HCO3£ |
| D£®ŌŚĆ÷·ÆČÜŅŗÖŠ¼ÓČėĒāŃõ»Æ±µČÜŅŗÖĮ³ĮµķÖŹĮæ“ļµ½×ī“󏱷¢ÉśµÄĄė×Ó·“Ó¦ŹĒ£ŗ 2Al3+ £«3SO42££«3Ba2+£«6OH££½ 3BaSO4”ż£«2 Al(OH)3”ż |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com