
| A. | 俄国化学家门捷列夫是通过实验的方法建立元素周期表的 | |
| B. | 现在我们课本上所列的元素周期表是由门捷列夫在1869年制定的 | |
| C. | 通常在元素周期表的右上方寻找制取催化剂的元素 | |
| D. | 元素的性质随着原子序数的递增而呈周期性变化 |
分析 A.门捷列夫是通过分析归纳的方法建立元素周期表的;
B.1869年俄国科学家门捷列夫绘制的元素周期表是元素依原子量大小并以表的形式排列,把有相似化学性质的元素放在同一行;
C.构成催化剂的元素为过渡金属元素;
D.根据周期表中元素的性质的变化规律分析.
解答 解:A.俄国化学家门捷列夫是通过分析归纳的方法汇出元素周期表的,不是通过实验的方法,故A错误;
B.1869年俄国科学家门捷列夫绘制的元素周期表是元素依原子量大小并以表的形式排列,把有相似化学性质的元素放在同一行.就是元素周期表的雏形.现代元素周期表依照核内正电荷(即质子数或原子序数)排列,故B错误;
C.构成催化剂的元素为过渡金属元素,在周期表过渡元素中寻找,故C错误;
D.在周期表中,元素的性质随着原子序数的递增而呈周期性变化,故D正确;
故选D.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置及性质为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可使溴水溶液褪色 | B. | 不能与酸性高锰酸钾溶液反应 | ||
| C. | 能发生银镜反应 | D. | 一定条件下能发生加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
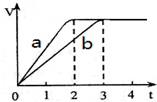 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图所示,下列说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图所示,下列说法正确的是( )| A. | 曲线a代表Al的反应过程,曲线b代表Mg的反应过程 | |
| B. | Mg和Al的质量之比为3:2 | |
| C. | Mg和Al的物质的量之比为3:2 | |
| D. | Mg和Al的反应速率之比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油不溶于水密度比水大 | B. | 石油中主要含有碳、氢两种元素 | ||
| C. | 石油的裂化属于物理变化 | D. | 石油分馏获得的各馏分是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
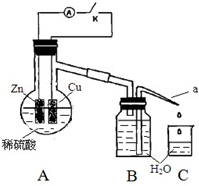 某同学分析Zn 与稀H2SO4的反应.
某同学分析Zn 与稀H2SO4的反应.| 1 分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1 分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C、O、S | B. | N、Na、Mg | C. | C、F、P | D. | N、O、P |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com