
 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图 所示.下列叙述中不正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图 所示.下列叙述中不正确的是( )| A、MOH是一种弱碱 |
| B、在x点,c(M+)=c(R+) |
| C、在x点,ROH完全电离 |
| D、稀释前,c(ROH)=10 c(MOH) |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、将氯化氢和SO2分别通入石蕊试液中,溶液都变为红色,所以它们都是酸类物质 |
| B、中和反应生成盐和水,有盐和水生成的反应一定是中和反应 |
| C、一氧化碳和氢气都能夺取氧化铜中的氧,它们都具有还原性 |
| D、离子是带电荷的原子或原子团,所以带电荷的微粒一定是离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+ NO3- CO32- Na+ |
| B、Na+ Ba2+ Mg2+ HCO3- |
| C、NO3- Mg2+ K+ Cl- |
| D、NO3- K+ AlO2- OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性氧化物,氧化亚铁,Fe2O3 |
| B、酸,硫酸,H2SO3 |
| C、碱,熟石灰,CaO |
| D、酸性氧化物,干冰,CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、②③④⑥⑨ |
| C、③④⑧⑨⑩ | D、②⑤⑦⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
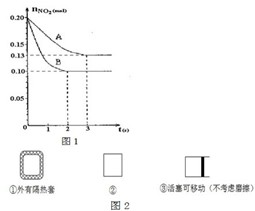 在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.
在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、冰、干冰、氯化钠、金刚石 |
| B、汞、钠、烧碱、二氧化硅 |
| C、NaCl、KCl、CsCl |
| D、H2O、H2S、H2Se、H2Te |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com