
| A. | 摩尔是物质的质量的单位 | |
| B. | 碳的摩尔质量为12g | |
| C. | 阿伏加德罗常数约为6.02×1023mol-1 | |
| D. | 一个碳原子的质量为12g |
分析 A、摩尔是物质的量的单位;
B、摩尔质量的单位为g/mol;
C、1mol物质中含有的微粒个数为阿伏伽德罗常数;
D、C的摩尔质量为12g/mol,即1mol碳的质量为12g,然后根据1mol碳中含NA个碳原子来分析计算.
解答 解:A、摩尔是物质的量的单位,物质的质量的单位为g,故A错误;
B、摩尔质量的单位为g/mol,故碳的摩尔质量为12g/mol,故B错误;
C、1mol物质中含有的微粒个数为阿伏伽德罗常数,故阿伏伽德罗常数为6.02×1023mol-1,故C正确;
D、C的摩尔质量为12g/mol,即1mol碳的质量为12g,1mol碳中含NA个碳原子,故1个碳原子的质量为$\frac{12g}{{N}_{A}}$=$\frac{12}{{N}_{A}}$g,故D错误.
故选C.
点评 本题考查了物质的量、物质的量的质量和摩尔质量的单位以及原子质量的计算等问题,难度不大,应注意基础的掌握.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | B. | 15N与14N互为同位素 | ||
| C. | 13C与C60互为同素异形体 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
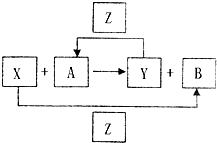 X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可).
X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
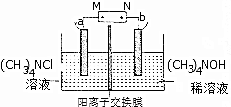 四甲基氢氧化铵常用作计算机硅片面用光亮剂和触刻剂,工业上以石墨为电极电解四甲基氯化铵溶液制备四甲基氢氧化铵 溶液的原理如图所示,下列说法不正确的是( )
四甲基氢氧化铵常用作计算机硅片面用光亮剂和触刻剂,工业上以石墨为电极电解四甲基氯化铵溶液制备四甲基氢氧化铵 溶液的原理如图所示,下列说法不正确的是( )| A. | b极为阴极,发生还原反应 | |
| B. | a处产生的气体能使湿润的淀粉碘化钾试纸变蓝 | |
| C. | 外电路电子的流向为M→a,b→N | |
| D. | 电解反应的总化学方程式为2(CH3)4NCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2(CH3)4NOH+H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
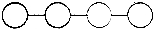
| A. | 若单体是4种氨基酸.则该化合物为四肽.其彻底水解后的产物再重新组合成四肽,共有24种排列方式 | |
| B. | 若单体是葡萄糖,则该化合物不能与斐林试剂发生特定的颜色反应 | |
| C. | 若单体是4种脱氧核苷酸,则该化合物彻底水解的产物是4个脱氧核糖、4个磷酸和4种碱基(A、O、G、C) | |
| D. | 若单体是4种核苷酸,则初步水解该化合物需要3个水分子. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
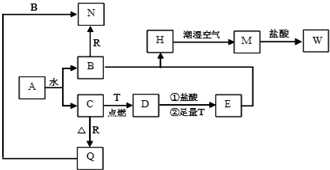
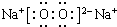 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 现象 | 化学反应方程式 | |
| ① | 试管中有白色沉淀生成 | Ba(NO3)2+CuSO4═BaSO4↓+Cu(NO3)2 |
| ② | 试管中有蓝色沉淀生成 | CuSO4+2NaOH═Cu(OH2)↓+2NaNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com