
下列关于反应能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)====ZnSO4(aq)+Cu(s) ΔH=-216 kJ·mol-1,反应物总能量<生成物总能量
B.相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol 氢分子的能量为E2,则2E1>E2
C.101 kPa时,2H2(g)+O2(g)====2H2O(g) ΔH=-483.6 kJ·mol-1, H2的燃烧热为241.8 kJ·mol-1
D.H+(aq)+OH-(aq)====H2O(l) ΔH=-57.3 kJ·mol-1,含1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ 的热量
科目:高中化学 来源: 题型:
有关甲烷和乙烷的说法中,错误的是( )
|
| A. | 互为同系物 |
|
| B. | 均不能使高锰酸钾酸性溶液褪色 |
|
| C. | 在核磁共振氢谱图(1H核磁共振谱图)中,均只有1个吸收峰 |
|
| D. | 二氯取代物均为两种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验测得某反应在不同pH下产物A的浓度随时间变化的关系如图(其他条件相同)。则下列有关说法正确的是( )
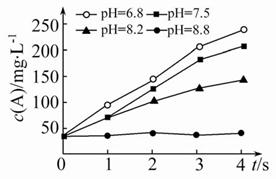
A.若增大压强,该反应的反应速率一定增大
B.pH=6.8时,随着反应的进行反应速率逐渐增大
C.一定pH范围内,溶液中H+浓度越小,反应速率越快
D.可采用调节pH的方法使反应停止
查看答案和解析>>
科目:高中化学 来源: 题型:
金属及其化合物在国民经济发展中起着重要作用。
(1)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:

该反应的氧化剂是_________,当生成19.2gCu时,反应中转移的电子为_____mol。铜在潮湿的空气中能发生吸氧腐蚀而生成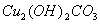 (碱式碳酸同)。该过程负极的电极反应式_______________。
(碱式碳酸同)。该过程负极的电极反应式_______________。
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(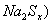 分别作为两个电极的反应物,固体
分别作为两个电极的反应物,固体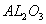 陶瓷(可传导
陶瓷(可传导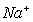 )为电解质,其原理如图所示:
)为电解质,其原理如图所示: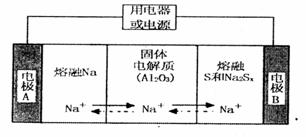
①根据下表数据,请你判断该电池工作的适宜温度应控制在_______。

②放电时,电极A为____极,S发生_______反应。
③放电时,内电路中的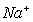 的移动方向为_______(填“从A到B”或“从B到A”)。
的移动方向为_______(填“从A到B”或“从B到A”)。
④充电时,总反应为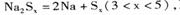 Na所在电极与直流电源_______极相连,阳极的电极反应式为________.
Na所在电极与直流电源_______极相连,阳极的电极反应式为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中正确的是( )
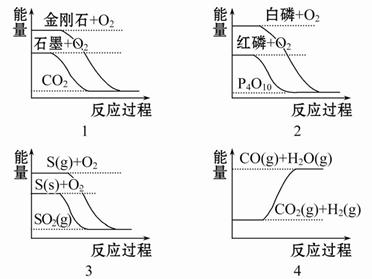
A.石墨转变为金刚石是吸热反应
B.白磷比红磷稳定
C.S(g)+O2(g)====SO2(g) ΔH1
S(s)+O2(g)====SO2(g) ΔH2 则ΔH1>ΔH2
D.CO(g)+H2O(g)====CO2(g)+H2(g) ΔH1>0
查看答案和解析>>
科目:高中化学 来源: 题型:
下列应用不涉及氧化还原反应的是
A.Na2O2用作呼吸面具的供氧剂
B.工业上电解熔融状态的Al2O3制备Al
C.工业上利用合成氨实现人工固氮
D.实验室用NH4Cl和Ca(OH)2制备NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在相同状况下,同一化学键断裂需要吸收的能量等于形成该化学键放出的能量。下列说法正确的是( )
A.电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应
B.水分解产生氢气和氧气时放出能量
C.相同状况下,反应2SO2+O2===2SO3是一个放热反应,则反应2SO3===2SO2+O2是一个吸热反应
D.氯化氢分解成氢气和氯气时放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是( )
A.稀NaOH溶液 B.HCl溶液
C.CuSO4溶液 D.酸性AgNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com