
| A、①② | B、①④ | C、②③ | D、③④ |


科目:高中化学 来源: 题型:
| △ |
| △ |
| A、C3N3(OH)3与HNCO虽最简式相同,但是两种不同的物质 |
| B、1mol HNCO与NO2反应时转移6mol电子 |
| C、HNCO是强还原剂 |
| D、N2既是氧化产物也是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、①③⑤ |
| C、②④⑧ | D、①⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NaCl的电子式: |
B、CO2的分子模型示意图: |
C、CrO5的结构式为: 该氧化物中Cr为+6价 该氧化物中Cr为+6价 |
| D、次氯酸的结构式:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验 | 实验现象 | 结论 |
| A | 广口瓶中光亮的铁钉放置一段时间后生锈 | 铁钉发生析氢腐蚀 |
| B | 左烧杯铝表面冒气泡,右烧杯铜表面冒气泡 | 活动性:Al>Fe>Cu |
| C | 左烧杯气体颜色加深,右烧杯气体颜色变浅 | NO2转化为N2O4吸热 |
| D | 白色固体先变为黄色,后变为黑色 | Ksp:AgCl>AgI>Ag2S |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、转移电子4.8NA个 |
| B、生成气体的体积42.56L(标准状况) |
| C、还原剂比氧化剂多0.2mol |
| D、被还原的氮原子是8.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
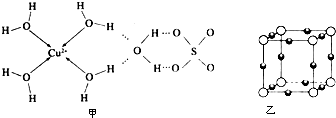
查看答案和解析>>
科目:高中化学 来源: 题型:
| Q | W | X | |
| Y | Z |
A、Q的一种核素中
| ||
| B、X的最高正化合价与最低负化合价的绝对值之差为6 | ||
| C、Y是常见的半导体材料 | ||
| D、Z的氧化物的水化物是强酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com