
 £»
£»·ÖĪö £Ø1£©ÓÉĀČŅŅĻ©ÖĘČ”¾ŪĀČŅŅĻ©£¬ŹĒĄūÓĆĢ¼Ģ¼Ė«¼üĻą»„¼Ó³É·“Ó¦ŹĒøß·Ö×Ó»ÆŗĻĪļ¾ŪĀČŅŅĻ©£»
£Ø2£©ĢśŗĶĮņĖįĶ·“Ӧɜ³ÉĮņĖįŃĒĢśŗĶĶ
£Ø3£©Ņ»Ńõ»ÆĢ¼¾ßÓŠ»¹ŌŠŌæÉŅŌ»¹ŌŃõ»ÆĢśÉś³ÉĢśŗĶ¶žŃõ»ÆĢ¼£»
£Ø4£©Ņ±Į¶½šŹōĀĮ£¬Ķس£²ÉÓƵē½āČŪČŚŃõ»ÆĀĮµÄ·½·Ø»ńµĆ£»
£Ø5£©½Ļ³¤Ģ¼Į“µÄĶéĢžĮŃ½āÉś³É½Ļ¶ĢĢ¼Į“µÄĶéĢžŗĶĻ©Ģž£®
½ā“š ½ā£ŗ£Ø1£©ĀČŅŅĻ©ŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬·¢Éś¼Ó¾Ū·“Ó¦£¬Éś³É¾ŪĀČŅŅĻ©»Æѧ·½³ĢŹ½£ŗnCH2=CHCl$”ś_{”÷}^{“߻ƼĮ}$ £¬
£¬
¹Ź“š°øĪŖ£ŗnCH2=CHCl$”ś_{”÷}^{“߻ƼĮ}$ £»
£»
£Ø2£©ĢśŗĶĮņĖįĶ·“Ӧɜ³ÉĮņĖįŃĒĢśŗĶĶ£¬»Æѧ·½³ĢŹ½ĪŖ£ŗFe+CuSO4=FeSO4+Cu£¬
¹Ź“š°øĪŖ£ŗFe+CuSO4=FeSO4+Cu£»
£Ø3£©Ņ»Ńõ»ÆĢ¼¾ßÓŠ»¹ŌŠŌ£¬Ņ»Ńõ»ÆĢ¼æÉŅŌ»¹ŌŃõ»ÆĢśÉś³ÉĢśŗĶ¶žŃõ»ÆĢ¼£¬»Æѧ·½³ĢĪŖ£ŗ3CO+Fe2O3$\frac{\underline{\;øßĪĀ\;}}{\;}$3CO2+2Fe£»
¹Ź“š°øĪŖ£ŗ3CO+Fe2O3$\frac{\underline{\;øßĪĀ\;}}{\;}$3CO2+2Fe£»
£Ø4£©ÓĆĀĮ·ÆĶĮ£ØAl2O3£©Ņ±Į¶ĀĮ£ŗµē½āČŪČŚŃõ»ÆĀĮæÉŅŌ»ńµĆĀĮŗĶŃõĘų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Al2O3 $\frac{\underline{\;µē½ā\;}}{\;}$4Al+3O2”ü£¬
¹Ź“š°øĪŖ£ŗ2Al2O3 $\frac{\underline{\;µē½ā\;}}{\;}$4Al+3O2”ü£»
£Ø5£©¶”ĶéŌŚŅ»¶ØĢõ¼žĻĀĮŃ½āÉś³ÉŅŅĻ©”¢ŅŅĶ飬·“Ó¦·½³ĢŹ½ĪŖ£ŗC4H10£Øg£© $”ś_{”÷}^{“߻ƼĮ}$C2H4+C2H6£¬
¹Ź“š°øĪŖ£ŗC4H10£Øg£© $”ś_{”÷}^{“߻ƼĮ}$C2H4+C2H6£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦·½³ĢŹ½µÄŹéŠ“£¬ĪŖøßĘµæ¼µć£¬Ć÷Č··“Ó¦ĪļÓėÉś³ÉĪļ¼“æɽā“š£¬×¢ŅāÕĘĪÕ³£¼ūµÄÓŠ»ś·“Ó¦ŌĄķ”¢³£¼ūĪŽ»śĪļµÄŠŌÖŹ£¬×¢ŅāÖŖŹ¶µÄ¹éÄÉŗĶÕūĄķ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖłÓĆNaOHŅŃ¾³±½ā | |
| B£® | ¶ØČŻŹ±¹Ū²ģŅŗĆęø©ŹÓ | |
| C£® | Ļ“µÓÉÕ±ŗĶ²£°ōµÄČÜŅŗĪ“×ŖČėČŻĮæĘæÖŠ | |
| D£® | ÓĆ“ųÓĪķĄµÄĶŠÅĢĢģĘ½³Ę2.4 g NaOHŹ±ĪóÓĆĮĖ”°×óĀėÓŅĪļ”±·½·Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆ·“Ó¦ÖŠµÄ»¹Ō¼ĮŹĒ S2O32- | |
| B£® | øł¾ŻøĆ·“Ó¦æÉÅŠ¶ĻŃõ»ÆŠŌ£ŗCl2£¾SO42- | |
| C£® | ÉĻŹö·“Ó¦ÖŠ£¬ĆæÉś³É 1 mol SO42-£¬æÉĶŃČ„2molCl2 | |
| D£® | øĆ·“Ó¦µÄŃõ»Æ²śĪļŹĒ Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
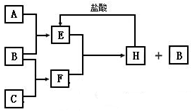 A”¢B”¢CŹĒ°“Ō×ÓŠņŹżÓÉŠ”µ½“óÅÅĮŠµÄµŚ¶ž”¢ČżÖÜĘŚŌŖĖŲµÄµ„ÖŹ£®B”¢E¾łĪŖ×é³ÉæÕĘųµÄ³É·Ö£®FµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£®ŌŚŅ»¶ØĢõ¼žĻĀ£¬ø÷ĪļÖŹÖ®¼äµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼£ØĶ¼ÖŠ²æ·Ö²śĪļĪ“ĮŠ³ö£©£ŗ
A”¢B”¢CŹĒ°“Ō×ÓŠņŹżÓÉŠ”µ½“óÅÅĮŠµÄµŚ¶ž”¢ČżÖÜĘŚŌŖĖŲµÄµ„ÖŹ£®B”¢E¾łĪŖ×é³ÉæÕĘųµÄ³É·Ö£®FµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£®ŌŚŅ»¶ØĢõ¼žĻĀ£¬ø÷ĪļÖŹÖ®¼äµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼£ØĶ¼ÖŠ²æ·Ö²śĪļĪ“ĮŠ³ö£©£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢśĖæŌŚĀČĘųÖŠČ¼ÉÕ£¬ĘææŚÓŠŗÖÉ«µÄĪķĘų | |
| B£® | ŌŚĪüČėÉŁĮæĀČĘųµÄÕėĶ²ÖŠĪüČėĒāŃõ»ÆÄĘČÜŅŗ£¬ČÜŅŗ±ä³ÉĒ³»ĘĀĢÉ« | |
| C£® | ĀČĖ®·Å¾ĆĮĖ»įÖš½„ÓÉ»ĘĀĢÉ«±ä³É¼øŗõĪŽÉ« | |
| D£® | äåĖ®ÖŠ¼ÓČėCCl4Õńµ“¾²ÖĆŗó£¬CCl4²ć¼øŗõĪŽÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆ£¾¾§Ģå¹č | B£® | NaCl£¾½šøÕŹÆ | C£® | MgO£¾l2 | D£® | CO2£¼SiO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1mol•L-1CH3COONaČÜŅŗÓė0.1mol•L-1CaCl2ČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØNa+£©+2c£ØCa2+£©ØTc£ØCH3COO-£©+c£ØCH3COOH£©+c£ØCl-£© | |
| B£® | ÅØ¶Č¾łĪŖ0.1mol•L-1µÄŠ”ĖÕ“ņČÜŅŗÓėÉÕ¼īČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØOH-£©-c£ØH+£©ØTc£ØHCO3-£©+c£ØH2CO3£© | |
| C£® | pHĻąĶ¬µÄ°±Ė®”¢KOHČÜŅŗ”¢Ba£ØOH£©2ČÜŅŗÖŠ£ŗc£ØNH4+£©£¼c£ØK+£©ØT2c£ØBa2+£© | |
| D£® | ³£ĪĀĻĀ£¬0.2mol•L-1NH4NO3ČÜŅŗÓė0.1mol•L-1NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆpHØT9.6µÄČÜŅŗÖŠ£ŗc£ØNO3-£©£¾c£ØNa+£©£¾c£ØNH4+£©£¾c£ØNH3•H2O£©£¾c£ØOH-£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
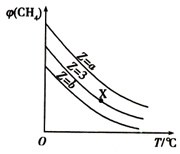 Ņ»¶ØĢõ¼žĻĀ£¬CH4ÓėH2O£Øg£©·¢Éś·“Ó¦CH4£Øg£©+H2O£Øg£©?CO£Øg£©+3H2£Øg£©£¬ÉčĘšŹ¼n£ØH2O£©/n£ØCH4£©=Z£¬ŌŚŗćŃ¹ĻĀ£¬Ę½ŗāŹ±¦Õ£ØCH4£©µÄĢå»ż·ÖŹżÓėZŗĶT£ØĪĀ¶Č£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
Ņ»¶ØĢõ¼žĻĀ£¬CH4ÓėH2O£Øg£©·¢Éś·“Ó¦CH4£Øg£©+H2O£Øg£©?CO£Øg£©+3H2£Øg£©£¬ÉčĘšŹ¼n£ØH2O£©/n£ØCH4£©=Z£¬ŌŚŗćŃ¹ĻĀ£¬Ę½ŗāŹ±¦Õ£ØCH4£©µÄĢå»ż·ÖŹżÓėZŗĶT£ØĪĀ¶Č£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆ·“Ó¦µÄģŹ±ä”÷H£¼0 | |
| B£® | Ķ¼ÖŠZµÄ“óŠ”ĪŖa£¼3£¼b | |
| C£® | Ķ¼ÖŠXµć¶ŌÓ¦µÄĘ½ŗā»ģŗĻĪļÖŠ$\frac{n£Ø{H}_{2}O£©}{n£ØC{H}_{4}£©}$=3 | |
| D£® | ĪĀ¶Č²»±äŹ±£¬Ķ¼ÖŠXµć¶ŌÓ¦µÄĘ½ŗāŌŚ¼ÓŃ¹ŗó¦Õ£ØCH4£©¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com