
【题目】常温下,用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的HX、HY溶液,pH随NaOH溶液体积变化如图。下列结论正确的是
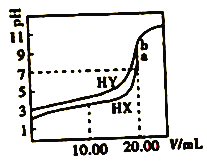
A. 水解常数:X->Y-
B. a、b两点溶液混合后:c(HX)+c(HY)+c(H+)=c(OH-)
C. pH=7时,c(Y-)>c(X-)
D. 10.00mlL时,有c(Na+)>c(HX)>c(X-)>c(H+)
【答案】B
【解析】分析:用浓度为0.1mol/L的NaOH溶液分别逐滴加入到20.00mL0.1mol/L的HX、HY溶液中,酸越弱,初始时刻pH值越大,根据图象可判断,酸性强弱为HY<HX;当NaOH反应了10.00mL时,溶液中分别存在HX-NaX和HY-NaY,且物质的量之比分别为1:1;当NaOH反应了20.00mL时,溶液中分别恰好存在NaX和NaY,二者均会发生水解使溶液呈碱性,根据图象和溶液中的守恒关系解答。
详解:A.对于HX和HY,酸性越弱,电离出的H+浓度越小,初始时刻根据图象,pH越小的酸酸性越强,电离程度就越大,因此酸性强弱为HY<HX,HX电离程度比HY更大,则水解常数X-<Y-,A错误;
B.当V(NaOH)=20.00 mL时,滴定HX的溶液中恰好存在NaX,滴定HY的溶液中恰好存在NaY,二者均水解溶液显碱性,根据质子守恒可知c(HX)+c(HY)+c(H+)=c(OH-),B正确;
C.pH=7时,溶液中c(H+)=c(OH-),根据电荷守恒,分别存在c(Na+)=c(X-),c(Na+)=c(Y-),但HX和HY此时消耗的NaOH的量不相同,前者消耗的多,因此c(X-)>c(Y-),C错误;
D.当V(NaOH)=10.00mL时,滴定HX的溶液中存在HX和NaX,物质的量之比为1:1,此时溶液显酸性,可以判断是酸的电离程度大于酸根离子的水解程度,对于HX-NaX溶液来说,根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(X-),由于溶液是酸性,因此c(H+)>c(OH-),则c(Na+)<c(X-),无论是电离还是水解,都是微弱的过程,因此X-、HX浓度都大于H+的浓度,所以溶液中粒子浓度大小关系为:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-),D错误;答案选B。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为2.0L的恒容密闭容器中分别加入一定量的X,发生反应:pX(g) ![]() Y(g)+Z(g),相关数据如下表所示:
Y(g)+Z(g),相关数据如下表所示:
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
X(g) | Y(g) | Z(g) | ||
Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | 0.160 | 0.160 |
Ⅲ | T | 0.20 | 0.090 | 0.090 |
回答下列问题:
(1)若容器Ⅰ中反应经10min达到平衡,则前10min内Y的平均反应速率v(Y)=___________。容器Ⅰ和容器Ⅱ中起始时X的反应速率v(X)Ⅰ___________v(X)Ⅱ(填“大于”“小于”或“等于”)。
(2)已知该正反应为放热反应,则T___________387(填“大于”或“小于”),判断理由是___________。
(3)反应方程式中X的化学计量数p的取值为___________,容器Ⅱ中X的平衡转化率为___________。若起始时向容器Ⅰ中充入0.1molX、0.15molY和0.10molZ,则反应将向___________ (填“正”或“逆”)反应方向进行,判断理由是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应,属于氧化还原反应的是( )
A. CaCO3![]() CaO + CO2 ↑ B. 2NaOH +CO2
CaO + CO2 ↑ B. 2NaOH +CO2![]() Na2CO3+ H2O
Na2CO3+ H2O
C. NaOH+HCl==NaCl+H2O D. 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年11月16日新闻报道“阿斯利康哮喘”新药获批上市,哮喘率降低近51%,有机物Z可用于治疗哮喘、系统性红斑狼疮等。其合成路线如下图所示
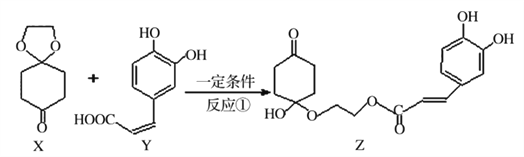
(1)化合物X的有_______种化学环境不同的氢原子。
(2)下列说法正确的是_______.
A.X是芳香化合物 B.Ni催化下Y能与5molH2加成
C.Z能发生加成、取代及消去反应 D. lmolZ最多可与5molNaOH反应
(3)Y与过量的溴水反应的化学方程式为_________。
(4)X可以由_______(写名称)和M(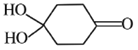 ) 分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N (分子式为C6H8O2),则N的结构简式为_____(己知烯醇式不稳定,会发生分子重排,例如:
) 分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N (分子式为C6H8O2),则N的结构简式为_____(己知烯醇式不稳定,会发生分子重排,例如: 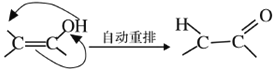 )。
)。
(5)Y也可以与环氟丙烷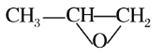 )发生类似反应①的反应,其生成物的结构简式为_________(写一种);Y的同分异构体很多种,其中有苯环、苯环上有二个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有_____种。
)发生类似反应①的反应,其生成物的结构简式为_________(写一种);Y的同分异构体很多种,其中有苯环、苯环上有二个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有_____种。
(6)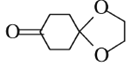 可由
可由 和有机物H分子间脱去一分子水而得,则H的名称为________;通常采用
和有机物H分子间脱去一分子水而得,则H的名称为________;通常采用![]() 为原料合成
为原料合成 ,请参照题目路线图设计该合成路线(无机试剂任选) _______。(合成路线常用的表示方式为:
,请参照题目路线图设计该合成路线(无机试剂任选) _______。(合成路线常用的表示方式为:  )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓氯水 | NaBr | 淀粉KI溶液 | 氧化性:Cl2>Br2>I2 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | Br2的苯溶液 | 铁屑 | AgNO3溶液 | 苯与溴单质在铁催化剂作用下 发生取代反应 | |
D | 硝酸 | Na2SO3 | KMnO4溶液 | SO2能使KMnO4溶液褪色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解正确的是( )
A. 1摩尔H2O质量为18g
B. 摩尔是国际科学界建议采用的一种物理量,简称摩,符号为 mol
C. 22.4LO 2 中所含氧气分子为1 摩尔
D. 1mol 氧含 6.02×10 23 个O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国北方生长的一种植物中含有抗菌作用的化合物M,已知M的合成路线如下图所示:
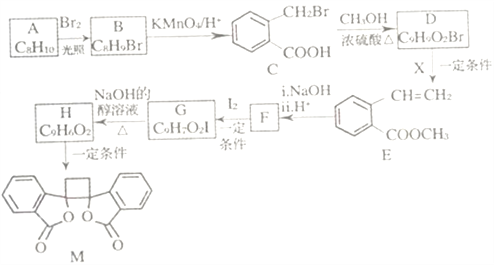
已知:i.RCH2Br![]() R-HC=CH-R';
R-HC=CH-R';
ii.R-HC=CH-R'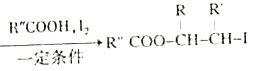 ;
;
iii.R-HC=CH-R'![]()
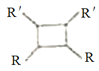 (以上R、R'、R"代表氢、烃基等)。
(以上R、R'、R"代表氢、烃基等)。
(1)A的化学名称为_______,D中所含官能团的名称是______。由H生成M的反应类型为_____。
(2)运用先进的分析仪器,极大改善了有机物结构鉴定。
①可利用_______(填“质谱”“红外光谱”或”核磁共振氢谱)测得C的相对分子质量。
②测定B的结构:B的核磁共振氢谱显示为_____组峰。
(3)1molM与足量NaOH溶液反应,消耗_____molNaOH。
(4)X的结构式为_____,F的结构简式为______ 。
(5)由C生成H的化学方程式为__________。
(6)符合下列条件的B的同分异构体共______种(不考虑立体异构)。
①芳香族化合物 ②与E具有相同官能团 ③能发生银镜反应 ④酸性条件下水解产物遇氯化铁溶液显紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
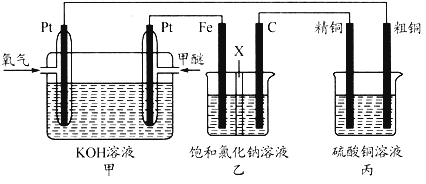
(1)通入氧气的电极为_____(填“正极”或“负极”),写出负极的电极反应式_____.
(2)铁电极为_____(填“阳极”或“阴极”),石墨电极的电极反应式为_____.
(3)反应一段时间后,乙装置中生成NaOH主要在_____(填“铁极”或“石墨极”)区.
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_____,反应一段时间,硫酸铜溶液浓度将_____(填“增大”“减小”或“不变”).
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为_____;丙装置中阴极析出铜的质量为_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是合成离分子树脂G和合成酚醛树酯的原料之一。相关的合成路线如下图所示:

已知:Ⅰ. (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
Ⅱ.![]()
请回答下列问题:
(1) 经质谱测定,有机物A的相对分子质量为164,燃烧8.2g有机物A,生成标准状况下11.2LCO2和5.4gH2O。则A的分子式是________,A中所含官能团的名称是________。
(2)B的结构简式________。
(3)C的名称是________,请写出在一定条件下C与足量新制氢氧化铜悬浊液反应的化学方程式________。
(4)D-F的反应类型是________,写出由C和苯酚合成酚醛树脂的化学方程式是___________。
(5)有机物![]() 有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式_________。
有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式_________。
Ⅰ.分子中除苯环外,无其它环状结构;
Ⅱ.核磁共振氯谱显示为5组峰;
Ⅲ.能发生水解反应,不能与Na反应
Ⅳ.能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com