
��250C 101KPa�����µ��Ȼ��⣨HCl������49.6L��ͨ��492mLˮ�У�����֪ˮ���ܶ�Ϊ��1.00g/mL�����õ��ܶ�Ϊ1.13g/mL�����ᣨ���Ȼ����ˮ��Һ����ע��250C 101KPa����������Ħ�����Ϊ24.8��/mol��(����������һλС��)
��1����������������������5�֣�
��2�������������ʵ���Ũ�ȣ���3�֣�
��3��ȡ��20.0 mL����Һ�����Ũ��Ϊ1.00 mol/L��ϡ��Һ����ϡ�ͺ���Һ������Ƕ��ٺ�������3�֣�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������KI��Һ��Ӧ������һ�ֿ�ʹ�����ǵ�ľ����ȼ�����塣��Ӧ�����Һ�е����̪����Һ���ɫ�������������Һ�����Ϊ��ɫ��Ϊ�ⶨ�����г����ĺ�������0��101kPa��33.6m3�Ŀ���ͨ��KI��Һ��ʹ֮��ȫ��Ӧ����������Һ����0.01mol��L-1��Na2S2O3��Һ60mLǡ����֮��Ӧ��ȫ����ӦʽΪ2Na2S2O3+I2 ![]() Na2S4O6+2NaI����
Na2S4O6+2NaI����
��1��������л�ѧ����ʽ��
O3+KI+H2O����
��2�����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(4��)��00C 101KPa�����µ��Ȼ��⣨HCl������44.8L��ͨ��492mLˮ�У�(��֪ˮ���ܶ�Ϊ��1.00g/mL),�õ��ܶ�Ϊ1.13g/mL�����ᣨ���Ȼ����ˮ��Һ����[
��1��������������������(����������һλС��)
��2�������������ʵ���Ũ�ȣ� (����������һλС��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�����ʡ�Ƹ��и�����ѧ����ĩ�������ۻ�ѧ�Ծ��������棩 ���ͣ������
ú�������Ǹ�Ч����������ú̿����Ҫ;��֮һ��
(1)��250C 101kPaʱ��H2��O2��������1mol H2O(g)�ų�241.8kJ�����������Ȼ�ѧ����ʽΪ
___________
��֪: ��C(s)��O2(g)�TCO2(g) ��H����393.5kJ/mol
��CO(g)��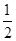 O2(g)�TCO2(g) ��H����283.0kJ/mol
O2(g)�TCO2(g) ��H����283.0kJ/mol
��̿��ˮ������Ӧ�ǽ�����ú��Ϊ����ȼ�ϵķ�����C(s)��H2O(g)�TCO(g)��H2(g) ��H=____kJ/mol
(2) CO������H2O(g)��һ��������Ӧ: CO(g)��H2O(g)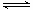 CO2(g)��H2(g) ��H��0�ں����ܱ������У���ʼʱn(H2O)=0.20mol��n(CO)��0.10 mol,��8000Cʱ�ﵽƽ��״̬��K��1.0����ƽ��ʱ��������CO��ת������_____________(����������һλС��)��
CO2(g)��H2(g) ��H��0�ں����ܱ������У���ʼʱn(H2O)=0.20mol��n(CO)��0.10 mol,��8000Cʱ�ﵽƽ��״̬��K��1.0����ƽ��ʱ��������CO��ת������_____________(����������һλС��)��
(3) ��ҵ�ϴ�ú������Ļ�����з����H2�����а��ĺϳɣ���֪��Ӧ��ӦN2(g)��3H2(g 2NH3(g)����H��0���ڵ��������½��У��ı�������Ӧ��������I��II��III����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��
2NH3(g)����H��0���ڵ��������½��У��ı�������Ӧ��������I��II��III����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��

��N2��ƽ����Ӧ����v1(N2)��vII(N2)��vIII(N2)�Ӵ�С���д���Ϊ________��
���ɵ�һ��ƽ��ڶ���ƽ�⣬ƽ���ƶ��ķ��� ��________����ȡ�Ĵ�ʩ��________��
�۱Ƚϵ�II�η�Ӧ�¶�(T2)�͵�III�η�Ӧ�ٶȣ�T3)�ĸߵͣ�T2________T3�����=��<���жϵ�������________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com