
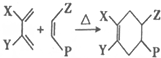
 .
. ;
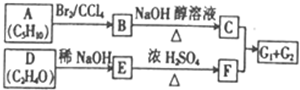
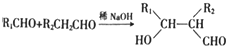
;分析 A能与溴反应,根据A的分子式可知,A有一个不饱和度,A的核磁共振氢谱有3组峰,峰面积比为6:3:1,所以A为(CH3)2C=CHCH3,根据各物质的转化关系,A与B发生加成反应生成溴代烃B为(CH3)2CBrCHBrCH3,B在氢氧化钠醇溶液中发生消去反应生成C为CH2=C(CH3)CH=CH2,D、E、F、G1、G2均能发生银镜反应,F中含甲基,根据D的分子式,结合信息⑤可知,D为CH3CHO,D发生加成反应生成E为CH3CHOHCH2CHO,E发生消去反应生成 F为CH3CHOH=CHCHO,G1、G2(均含六元环)互为同分异构体,根据信息④可知,C和F发生加成反应生成G1、G2为 ,据此答题.
,据此答题.
解答 解:A能与溴反应,根据A的分子式可知,A有一个不饱和度,A的核磁共振氢谱有3组峰,峰面积比为6:3:1,所以A为(CH3)2C=CHCH3,根据各物质的转化关系,A与B发生加成反应生成溴代烃B为(CH3)2CBrCHBrCH3,B在氢氧化钠醇溶液中发生消去反应生成C为CH2=C(CH3)CH=CH2,D、E、F、G1、G2均能发生银镜反应,F中含甲基,根据D的分子式,结合信息⑤可知,D为CH3CHO,D发生加成反应生成E为CH3CHOHCH2CHO,E发生消去反应生成 F为CH3CHOH=CHCHO,G1、G2(均含六元环)互为同分异构体,根据信息④可知,C和F发生加成反应生成G1、G2为 ,
,
(1)A为(CH3)2C=CHCH3,A的名称为2-甲基-2-丁烯,根据上面的分析可知,E→F的反应类型是消去反应,
故答案为:2-甲基-2-丁烯;消去反应;
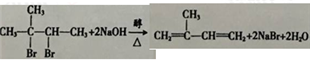
(2)B→C为溴代烃的消去反应,反应的化学方程式为 ,
,
故答案为: ;
;
(3)根据上面的分析可知,D的结构简式为CH3CHO,
故答案为:CH3CHO;
(4)根据上面的分析可知,G1、G2 结构简式分别为 ,G1、G2的元素组成相同,故选c,
,G1、G2的元素组成相同,故选c,
故答案为: ; c;
; c;
(5)E为CH3CHOHCH2CHO,与E互为同分异构体且能发生银镜反应即有醛基的异构体为CH3CH2CHOHCHO、CH2OHCH2CH2CHO、(CH3)2COHCHO、CH2OHCH(CH3)CHO、HCOOCH2CH2CH3、HCOOCH(CH3)2,有6种(不含立体结构,不含醚键),其中核磁共振氢谱有3组峰且面积比为6:1:1的为(CH3)2COHCHO、HCOOCH(CH3)2,
故答案为:6;(CH3)2COHCHO、HCOOCH(CH3)2.
点评 本题考查有机物的推断与合成,注意充分利用有机物的结构特点、分子式与反应条件进行推断,熟练掌握官能团的性质与转化是解答本题的关键,题目难度中等


科目:高中化学 来源: 题型:选择题
| A. | SiO32-、Br-、K+、Na+ | B. | NH4+、SO42-、Cl-、NO3- | ||
| C. | K+、Na+、ClO-、Cl- | D. | K+、SO42-、HCO3-、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
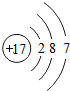 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | 评价及离子方程式 |
| A | H+、Fe2+、NO3-、Cl- | 不能大量共存于同一溶液中,因为发生反应:Fe2++2H+=Fe3++H2↑ |
| B | Na+、K+、HCO3-、OH- | 不能大量共存于同一溶液中,因为发生反应:HCO3-+OH-=H2O+CO2↑ |
| C | Ca2+、NH4+、CO32-、Cl- | 能大量共存于同一溶液中 |
| D | Na+、NH4+、SO42-、Cl- | 能大量共存于同一溶液中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol钠与过量盐酸反应生成NA个H2分子 | |
| B. | 金属钠加到冷水中,反应的离子方程式是:Na+2H2O═Na++OH-+H2↑ | |
| C. | 1molNa2O2与足量的水反应,转移电子数为2NA个 | |
| D. | 为测定熔融NaOH的导电性,可在瓷坩埚中熔化NaOH固体后进行测量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cu2+、Cl-、OH- | B. | Mg2+、SO42-、K+、Cl- | ||
| C. | Na+、H+、NO3-、CO32- | D. | Ba2+、Na+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaHSO4固体是离子晶体 | |
| B. | NaHSO4晶体中阳离子和阴离子的个数是2:1 | |
| C. | NaHSO4晶体熔化时破坏的是离子键和共价键 | |
| D. | NaHSO4固体溶于水时既破坏离子键又破坏共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com