
| 选项 | 性质 | 实际应用 |
| A | 活性炭可吸附水中的悬浮物 | 用于自来水的杀菌消毒 |
| B | SO2具有还原性 | 漂白纸浆 |
| C | 铁被氧气氧化时会放出热量 | 铁、活性炭、无机盐、水等的混合物制成暖宝贴 |
| D | 氧化铝是两性氧化物 | 作耐高温材料 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.物质能杀菌消毒一般具有氧化性,能够使蛋白质变性;
B.依据二氧化硫的漂白性解答;
C.铁粉、活性炭、无机盐等形成原电池反应,发生氧化反应放出热量;
D.耐高温材料应具有较高的熔点.
解答 解:A.活性炭具有吸附性,能够净水,不具有强氧化性,不能用于杀菌消毒,故A错误;
B.二氧化硫漂白纸浆是因为其具有漂白性,与其还原性无关,故B错误;
C.铁与氧气、水形成原电池反应,发生氧化反应,放出热量,可以用此反应制暖宝贴,故C正确;
D.氧化铝作耐高温材料是因为其具有较高的熔点,与氧化铝的两性无关,故D错误;
故选:C.
点评 本题考查了元素化合物知识,侧重考查元素化合物的用途,明确相关物质的性质是解题关键,注意盐类水解的应用,题目难度不大.


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:选择题
| A. | 放电时,电解质溶液中K+移向负极 | |
| B. | 放电时,电解质溶液的pH 不变 | |
| C. | 充电时,阴极的反应为:Zn(OH)42-+2e-=Zn+4OH- | |
| D. | 充电时,当有4.48L 氧气(标准状况下)释放出来时,则析出固体Zn为13g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 元素性质或原子结构信息 |
| Q | 原子核外有6种不同运动状态的电子 |
| R | 最外层电子数是次外层电子数的3倍 |
| X | 气态氢化物的水溶液呈弱碱性 |
| Y | 第三周期元素的简单离子中离子半径最小 |
| Z | 单质为银白色固体,在空气中燃烧发出黄色火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向25mL沸水中滴加5~6滴FeCl3饱和溶液立刻出现红褐色沉淀 | |
| B. | Na、Mg、AL的最高价氧化物水化物的碱性逐渐增强 | |
| C. | 1-丙醇、2.丙醇的消去产物的核磁共振氢谱图不同 | |
| D. | 2.3gNa与氧气完全反应,转移的电子数为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.075mol/L | B. | 0.1125mol/L | C. | 0.15mol/L | D. | 0.225mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
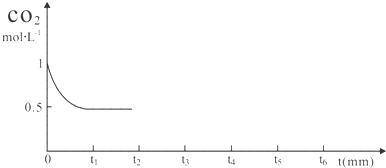
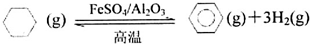
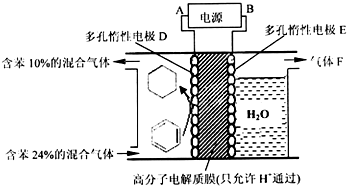
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氯储存在钢瓶中 | B. | 液溴装入试剂瓶中应加少量水液封 | ||
| C. | 固体碘保存在CCl4中 | D. | 氢氟酸盛放在塑料瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com