
| A. | 有Cu生成的一极是阴极,发生氧化反应 | |
| B. | 反应中转移电子的物质的量为0.4 mol | |
| C. | 在另一极得到O2的体积(标准状况)是1.12 L | |
| D. | 电解一段时间后,溶液的pH不变 |
分析 电解硫酸铜溶液,阳极发生氧化反应,电极方程式为4OH--4e-=2H2O+O2↑,阴极发生还原反应,电极方程式为2Cu2++4e-=2Cu,结合生成铜的质量计算转移电子的物质的量,进而可确定溶液的pH以及氧气的体积.
解答 解:A.有Cu生成的一极是阴极,发生还原反应,故A错误;
B.阴极发生还原反应,电极方程式为2Cu2++4e-=2Cu,n(Cu)=$\frac{6.4g}{64g/mol}$=0.1mol,则转移电子的物质的量为0.2mol,故B错误;
C.转移电子0.2mol,阳极反应为4OH--4e-=2H2O+O2↑,可知生成氧气0.05mol,体积为0.05mol×22.4L/mol=1.12L,故C正确;
D.反应过程中消耗氢氧根离子使溶液中氢离子浓度增大,也就是放氧生酸,pH会减小,故D错误;
故选C.
点评 本题考查了电极原理的分析应用,电子守恒的计算应用,电极判断和计算是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 先加BaCl2,再加入HCl | B. | 先加HNO3,再加BaCl2 | ||
| C. | 先加H2SO4,再加BaCl2 | D. | 先加HCl,再加BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌 | |
| B. | 可用酒精萃取碘水中的I2 | |
| C. | 在碘水中加入几滴淀粉溶液,溶液变蓝色 | |
| D. | 含I-的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
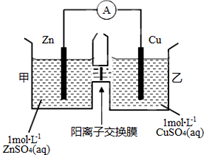 锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )| A. | Zn电极上发生氧化反应 | |
| B. | 电子的流向为Zn→电流表→Cu | |
| C. | SO42-由乙池通过离子交换膜向甲池移动 | |
| D. | 电池工作一段时间后,乙池溶液的总质量明显增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
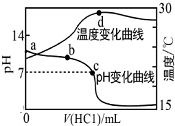 室温下,向a点(pH=a)的20.00mL 1.000mol•L-1氨水中滴入1.000mol•L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法错误的是( )
室温下,向a点(pH=a)的20.00mL 1.000mol•L-1氨水中滴入1.000mol•L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法错误的是( )| A. | 将此氨水稀释,溶液的导电能力减弱 | |
| B. | b点溶液中离子浓度大小可能存在:c(NH${\;}_{4}^{+}$)>c(Cl-)>c(OH-)>c(H+) | |
| C. | c点时消耗盐酸体积V(HCl)<20.00mL | |
| D. | a、d两点的溶液,水的离子积Kw(a)>Kw(d) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
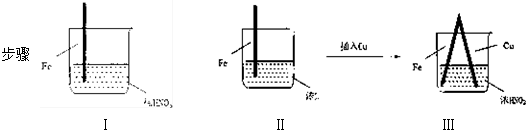
| A. | Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| X | ||
| Y | ||
| Z |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com