
����Ŀ����ͼ��ʾ��װ�ã�����һ�ֿɳ���أ�װ�ã���Ϊ���أ�װ�ã������ӽ���Ĥֻ����Na+ͨ������س䡢�ŵ�Ļ�ѧ����ʽΪ��
2Na2S2+NaBr3 ![]() Na2S4+3NaBr�����պ�Kʱ��X��������Һ���ɫ��
Na2S4+3NaBr�����պ�Kʱ��X��������Һ���ɫ��
����˵����ȷ���ǣ� ��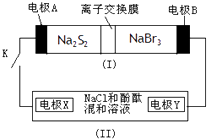
A.װ�ã�I����Na+���ҵ���ͨ�����ӽ���Ĥ
B.A�缫�ĵ缫��ӦʽΪ��NaBr3+2Na++2e��=3NaBr
C.X�缫�ĵ缫��ӦʽΪ��2Cl����2e��=Cl2��
D.ÿ��0.1mol Na+ͨ�����ӽ���Ĥ��X�缫�Ͼ����ɱ�״��������1.12L
���𰸡�D
���������⣺A��ԭ������������������ƶ�����պ�Kʱ�������Ӵ�����ͨ�����ӽ���Ĥ����A����B���պ�Kʱ��AΪԭ��صĸ�������������������Ӧ���缫��ӦΪ2Na2S2��2e��=2Na++Na2S4 �� ��B����
C���պ�Kʱ��X��������Һ���ɫ��˵��X������OH�����ӣ�Ϊ���ص�������������ӦΪ2H2O+2e��=H2��+2OH�� �� ��C����
D���պ�Kʱ����0.1molNa+ͨ�����ӽ���Ĥ��˵����0.1mol����ת�ƣ�����������0.05molH2 �� ��״�������Ϊ0.05mol��22.4L/mol=1.12L����D��ȷ��
��ѡD��


 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧ������ͼ��ʾװ��̽������������������ʣ� 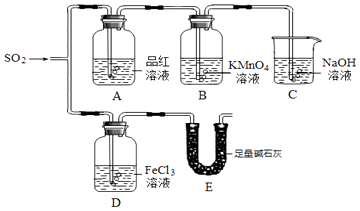
��ش�
��1������E�������� �� ��û��װ��C��������ֱ���ŷŵ������У����������Ҫ���������� ��
��2���۲쵽B����Һ��ɫ��dz��˵����SO2���е���������
��3��д������D�е�ʵ������ �� ����������ԭ��Ӧ�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʻ�Ϊͬ���칹�����
A. ����������
B. ��������ϩ
C. ��ϩ���ϩ
D. ���������춡��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ԭ��������������Ⱦ�����й㷺��Ӧ�ã���ҵ�ϳ�������ͼ��ʾ���װ�ã��������Ļ�������[Fe��CN��6]3���ɽ���̬�������е�����ת��Ϊ�����õ�������ת��Ϊ[Fe��CN��6]4�� �� ͨ���⣬Ȼ��ͨ��H2S���Դ���������˵������ȷ���ǣ� �� 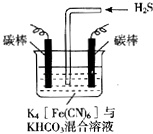
A.���ʱ������ӦʽΪ[Fe��CN��6]4����e��=[Fe��CN��6]3��
B.����������������Һ��pH���
C.������������Ҫ���ϲ���K4[Fe��CN��6]��KHCO3
D.ͨ��H2Sʱ������Ӧ�����ӷ���ʽΪ��2[Fe��CN��6]3��+2CO32��+H2S=2[Fe��CN��6]4��+2HCO3��+S��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧ��ӦA2��g��+B2��g���T2AB��g���������仯��ͼ��ʾ���ж�������������ȷ���ǣ� �� 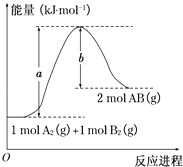
A.ÿ����2����AB����b kJ����
B.�÷�Ӧ�ȡ�H=+��a��b��kJmol��1
C.�÷�Ӧ�з�Ӧ��������������������������
D.����1 mol A��A��1 mol B��B�����ų�a kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��TiO2�ڹ�ҵ�������ճ�����������Ҫ��;��
��1����ҵ����������ʯ��FeTiO3 �� ��FeO��Al2O3��SiO2�����ʣ�����������Ӧ�Ƶã� 
���У�����۷����ķ�ӦΪ��2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O��
��i�������ѿ�ʯʱ������Ũ����������Һ��������д���ù������������������Ӧ�����ӷ�Ӧ����ʽ�� ��
��ii��������X������
��iii���ܢ�������Ŀ���� ��
��iv��д���Ļ�ѧ��Ӧ����ʽ ��
��2��TiO2��ͨ���������ַ����Ʊ������ѣ�����һ���Ƚ�TiO2��Cl2��C��Ӧ�õ�TiCl4 �� ����þ��ԭ�õ�Ti��
��i��д������TiCl4�Ļ�ѧ��Ӧ����ʽ
�������ǵ��TiO2�����Ti��ͬʱ����O2����
����������TiO2��������ʯīΪ����������CaOΪ���Һ����̼�������۳أ�
��ii��������Ӧ�ĵ缫��ӦʽΪ ��
��iii�����������趨������۳��м���̼���ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL 0.50mol/L������50mL 0.55mol/L NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺ 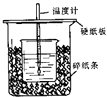
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ�� ��
��2���ձ���������ֽ���������� ��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ���ƫ��ƫС����Ӱ�족��
��4�������60mL 0.50mol/L������50mL 0.55mol/L NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������������ȡ�����ȡ����������к��������ȡ�����ȡ�������������
��5������ͬŨ�Ⱥ�����İ�ˮ��NH3H2O������NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ�������ƫ����ƫС��������Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��ҺX�У����ܺ���Na+��Cu2+��Mg2+��Al3+��SiO32����AlO2����CO32����Cl���е�һ�ֻ��֣���ȡ����Һ�����������м���һ�����ʵ���Ũ�ȵ�ϡ���ᣬ�������������ʵ�����n�����������������V���Ĺ�ϵ��ͼ��ʾ������˵���в���ȷ���ǣ� �� 
A.��ҺX��һ������Cu2+��Mg2+��Al3+ �� ���ܺ���Cl��
B.OA�βμӷ�Ӧ�������ӵ����ʵ���֮��Ϊ2��1��1��2
C.AB��һ������������
D.BC�η�����Ӧ�����ӷ���ʽΪ��Al��OH��3+3H+=Al3++3H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com