
【题目】钢铁分析中常用高氯酸(HClO4)溶解矿样,某研究性学习小组欲制备少量高氯酸。该学习小组查阅到:a.HClO4浓度高于60%时遇含碳化合物易爆炸,浓度低于60%时比较稳定;b.NaClO4与浓硫酸反应可制得高氯酸,若采用真空蒸馏可得纯高氯酸;c.NaClO3 在673K(400℃)分解产生NaClO4、NaCl和一种气体。该小组同学设计实验分三步制备高氯酸;(一)制氯气并使制得的氯气与氢氧化钠溶液反应制氯酸纳;(二)氯酸钠分解制高氯酸钠;(三)高氯酸纳与浓硫酸反应制高氯酸[2NaClO4+H2SO4(浓) ![]() Na2SO4+2HClO4 ]。
Na2SO4+2HClO4 ]。
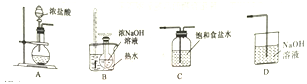
(1)制取氯酸钠的装置连接顺序为A,____________。由装置可知该小组制氯气时采用的氧化剂可以为___________(填化学式)。
(2)B装置中发生反应的离子方程式为_________________________。
(3)为了制备高氯酸钠并推出氯酸钠分解制高氯酸钠的化学方程式,该小组设计了两组装置(甲,乙)如下:

该小组经过分析决定选用甲装置制备高氯酸钠,取NaClO3样品2.13 g,加热充分反应后集气瓶中收集到224 mL(标准状况下)气体,则该反应的化学方程式为_____________________;不选用乙装置的原因可能为____________________。
(4)用丙装置制备高氯酸,向烧瓶中加入高氯酸钠,然后加入浓硫酸后,加热可制取高氯酸。实验开始前,胶塞及导管接口需要包锡箔纸,其原因是_________________,仪器E的名称为________。该组同学发现操作中少加入一种物质,该物质的名称为________。发现后的正确操作为_____________。
(5)工业上大量制备NaClO4 常用高电流密度电解NaClO3 的方法,试写出以惰性电极电解时的阳极反应式:___________________________________。
【答案】 C,B,D KMnO4 Cl2+ 6OH-![]() 5Cl- +ClO3-+3H2O 2NaClO3
5Cl- +ClO3-+3H2O 2NaClO3![]() NaClO4+NaCl+O2 乙装置不能快速判断氯酸钠是否完全反应且反应后气体无法收集 橡胶中含有“碳”,若生成的高氯酸浓度高时遇胶塞及导管极有可能会爆炸 锥形瓶 碎瓷片(或沸石) 停止实验,冷却后加入碎瓷片(或沸石)再继续进行实验 ClO3--2e+H2O==ClO4-+2H+
NaClO4+NaCl+O2 乙装置不能快速判断氯酸钠是否完全反应且反应后气体无法收集 橡胶中含有“碳”,若生成的高氯酸浓度高时遇胶塞及导管极有可能会爆炸 锥形瓶 碎瓷片(或沸石) 停止实验,冷却后加入碎瓷片(或沸石)再继续进行实验 ClO3--2e+H2O==ClO4-+2H+
【解析】本题主要考查对于制备高氯酸探究实验的评价。
(1)A制取的氯气通过C除去氯化氢杂质,在B制得的氯气与氢氧化钠溶液反应制氯酸纳,用D吸收氯气的余气,防止污染环境,所以制取氯酸钠的装置连接顺序为A,C,B,D。制取氯气的装置不需要加热,由装置可知该小组制氯气时采用的氧化剂可以为KMnO4。
(2)B装置中发生反应的离子方程式为Cl2+6OH-![]() 5Cl-+ClO3-+3H2O。
5Cl-+ClO3-+3H2O。
(3)该小组经过分析决定选用甲装置制备高氯酸钠,2.13gNaClO3样品的物质的量为0.02mol,224mL(标准状况下)气体的物质的量为0.01mol,则该反应的化学方程式为2NaClO3![]() NaClO4+NaCl+O2;不选用乙装置的原因可能为乙装置不能快速判断氯酸钠是否完全反应且反应后气体无法收集。
NaClO4+NaCl+O2;不选用乙装置的原因可能为乙装置不能快速判断氯酸钠是否完全反应且反应后气体无法收集。
(4)实验开始前,胶塞及导管接口需要包锡箔纸,其原因是橡胶中含有“碳”,若生成的高氯酸浓度高时遇胶塞及导管极有可能会爆炸,仪器E的名称为锥形瓶。该组同学发现操作中少加入一种物质,该物质的名称为碎瓷片(或沸石)。发现后的正确操作为停止实验,冷却后加入碎瓷片(或沸石)再继续进行实验。
(5)以惰性电极电解时的阳极反应式:ClO3--2e+H2O==ClO4-+2H+。


科目:高中化学 来源: 题型:
【题目】雾霾是对空气中各种悬浮颗粒物含量超标的笼统表述,而氮氧化物是造成酸雨和光化学烟雾的罪魁祸首之一,工业上在一定温度和催化剂条件下,NH3可用于消除NO的污染,生成一种无害气体。
(1)悬浮颗粒物可用高压电除去,利用了________________现象。
(2)实验室制备氨气的原理:_________________________(用化学方程式表示)。反应发生、气体收集和尾气处理的装置依次为_______(填序号)。

(3)实验室也可采用下图所示装置制取氨气。烧瓶内可选用______________(填序号)。

A.NaOH固体 B.无水氯化钙 C.二氧化硅 D.碱石灰
(4)按下图装置进行NH3性质实验。

①先打开旋塞1,B瓶中的现象是_____________________,原因是______________________,稳定后,关闭旋塞1。
②再打开旋寒2,B瓶中的现象是_____________________________。
(5)请写出NH3与NO2反应的化学方程式:_______________________。该反应中每生成1nolN2转移的电子数____________________(结果保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)①按系统命名法,化合物 ![]() 的名称是
的名称是
②二乙酸乙二酯的结构简式: .
(2)苯的同系物A,分子中共含66个电子,A苯环上一溴代物只有一种,A的结构简式为 .
(3)C5H4理论上同分异构体的数目可能有30多种,如:A.CH2=C=C=C=CH2 B.CH≡C﹣CH=C=CH2 C. ![]() D.
D. ![]() ,其中A、B是链状分子(不考虑这些结构能否稳定存在),请写出所有碳原子均共线的一种链状分子的结构简式: .
,其中A、B是链状分子(不考虑这些结构能否稳定存在),请写出所有碳原子均共线的一种链状分子的结构简式: .
(4)![]() 分子中最多有个原子共面.
分子中最多有个原子共面.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银锌电池广泛用作各种电子仪器的电源,它的电池反应是Zn+Ag2OH2O=2Ag+Zn(OH)2则负极上发生反应的物质是( )
A.Ag
B.Zn(OH)2
C.Ag2O
D.Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的相对分子质量为58,请回答:
(1)若该有机物为烃,且含有支链,则其名称为 .
(2)若为结构中只含1个﹣CH3和一个官能团的含氧衍生物,则官能团的名称为 .
(3)若为结构中有2个﹣CH3含氧衍生物,则可能的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某有机物合成反应的流程图: 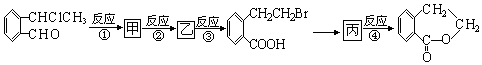
已知甲溶液遇石蕊溶液变红.请回答下列问题:
(1)有机物丙中官能团的名称为 .
(2)写出下列反应的化学方程式及反应类型
反应① , .
反应② , .
(3)![]() →丙实际需要两步才能完成,写出第一步反应的化学方程式 , 第二步所用试剂及目的是 .
→丙实际需要两步才能完成,写出第一步反应的化学方程式 , 第二步所用试剂及目的是 .
(4)丙有多种同分异构体,其中符合下列条件的同分异构体共有种,写出其中苯环上一氯代物有两种的有机物的结构简式 .
a、遇FeCl3溶液显色b、能发生银镜反应及水解反应c、苯环上只有2个取代基.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是
A. 锌粒与稀硫酸的反应 B. 灼热的木炭与CO2的反应
C. 甲烷在空气中燃烧的反应 D. Ba(OH)28H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所涉及的物质均为中学化学中的常见物质,其中C、D均为气体单质,E是固体单质,A物质的焰色反应火焰为紫色,F是黑色晶体,它们存在如图转化关系,反应中生成的水及次要产物均的已略去。

(1)写出下列物质的化学式:C_____________,D______________,H____________。
(2)指出MnO2在相关反应中的作用:反应①中做_______剂,反应②中做_________剂。
(3)当①中有1molA完全反应时转移电子的物质的量是________mol。
(4)检验G中阳离子的方法_________________________________________ 。
(5)保存G溶液时为什么要加固体E_____________________________________。
(6)写出F→G+H的离子方程式:____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com