
【题目】氨在工农业生产中应用广泛,可由N2、H2合成NH3。
(1)天然气蒸汽转化法是前获取原料气中H2的主流方法。CH4经过两步反应完全转化为H2和CO2,其能量变化示意图如下:

结合图像,写出CH4通过蒸汽转化为CO2和H2的热化学方程式______________________。
(2)利用透氧膜,一步即获得N2、H2,工作原理如图所示(空气中N2与O2的物质的量之比按4∶1计)
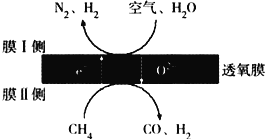
①起还原作用的物质是_________________________。
②膜I侧所得气体![]() =2,CH4、H2O、O2反应的化学方程式是______________________。
=2,CH4、H2O、O2反应的化学方程式是______________________。
(3)甲小组模拟工业合成氨在一恒温恒容的密闭容器中发生如下反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH< 0。t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示,下列说法正确的是____________
2NH3(g) ΔH< 0。t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示,下列说法正确的是____________

A.Ⅰ、Ⅱ两过程到达平衡时,平衡常数:KⅠ<KⅡ
B.Ⅰ、Ⅱ两过程到达平衡时,NH3的体积分数:Ⅰ<Ⅱ
C.Ⅰ、Ⅱ两过程到达平衡的标志:混合气体密度不再发生变化
D.t2时刻改变的条件可以是向密闭容器中加N2和H2混合气
(4)乙小组模拟不同条件下的合成氨反应,向容器充入9.0molN2和23.0molH2,图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。
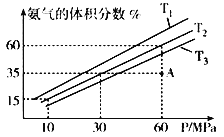
①T1、T2、T3由大到小的排序为______________________________。
②在T2、60MPa条件下,比较A点v正___v逆(填“>”、“<”或“=”),理由是____________。
③计算T2、60Mpa平衡体系的平衡常数Kp=__________。(用平衡分压代替平衡浓度计算,分压=总压x物质的量分数)
【答案】 CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H=+165.4 kJ/mol CH4 10CH4+8H2O+O2=10CO+28H2 D T3>T2>T1 > 在T2、60Mpa 时A点未达到平衡时的体积分数,反应向正向进行,所以v(正)>v(逆) 0.043(MPa)-2或 0.0427(MPa)-2
【解析】(1)根据图像得到热化学方程式Ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4kJ/mol,Ⅱ.CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.0kJ/mol,结合盖斯定律计算Ⅰ+Ⅱ得到1mol CH4(g)通过蒸汽转化为CO2(g)和H2(g)的热化学方程式:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.4 kJ/mol,故答案为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.4kJ/mol;
(2)①甲烷中C失去电子生成CO,则起还原作用的物质是CH4,故答案为:CH4;
②空气中N2与O2的物质的量之比为4:1,膜Ⅰ侧所得气体![]() =2,氮气在反应前后不变,设氮气为4mol,则生成氢气为8mol,膜Ⅰ侧发生的电极反应式是H2O+2e-=H2+O2-、O2+4e-=2O2-,由膜I侧反应可知8molH2O得到16mol电子、1molO2得到4mol电子,共得到20mol电子,膜II上1molCH4中C失去6mol电子、H得到4mol电子,即1molCH4失去2mol电子,根据总反应遵循电子守恒,需要10molCH4反应,则反应为10CH4+8H2O+O2=10CO+28H2,故答案为:10CH4+8H2O+O2=10CO+28H2;
=2,氮气在反应前后不变,设氮气为4mol,则生成氢气为8mol,膜Ⅰ侧发生的电极反应式是H2O+2e-=H2+O2-、O2+4e-=2O2-,由膜I侧反应可知8molH2O得到16mol电子、1molO2得到4mol电子,共得到20mol电子,膜II上1molCH4中C失去6mol电子、H得到4mol电子,即1molCH4失去2mol电子,根据总反应遵循电子守恒,需要10molCH4反应,则反应为10CH4+8H2O+O2=10CO+28H2,故答案为:10CH4+8H2O+O2=10CO+28H2;
(3)A、由图象分析可知,平衡常数是温度的函数,温度不变平衡常数不变,故A错误;B、t2时刻改变条件后达到平衡时,逆反应速率增大,不能说明平衡移动的方向,无法判断氨气体积分数的变化,故B错误;C、容器的体积不变,气体的质量不变,气体的密度始终不变,不能用于平衡的判断,故C错误;D、t2时刻,向密闭容器中加H2和N2混合气,气体的压强增大,逆反应速率增大,故D正确;故选D;
(4)①N2(g)+3H2(g)![]() 2NH3(g) ΔH< 0,相同压强下,升高温度平衡逆向移动,氨气的体积分数减小,根据图知,温度由大到小的顺序为T3>T2>T1,故答案为:T3>T2>T1;
2NH3(g) ΔH< 0,相同压强下,升高温度平衡逆向移动,氨气的体积分数减小,根据图知,温度由大到小的顺序为T3>T2>T1,故答案为:T3>T2>T1;
②根据图像,在T2、60MPa条件下,A点为达到平衡状态,要达到平衡,反应需要继续正向进行,因此v正>v逆,故答案为:>;在 T2、 60Mpa 时A点未达到平衡时的体积分数,反应向正向进行,所以 v(正)>v(逆);
③若体系在T2、60MPa下达到平衡,相同温度下,气体的体积分数等于其物质的量分数,
设平衡时n(NH3)=xmol,
N2(g) + 3H2(g)2NH3(g)
开始(mol) 9 23 0
反应(mol) 0.5x 1.5x x
平衡(mol)9-0.5x 23-1.5x x
平衡时氨气体积分数=![]() ×100%=60%,解得x=12,氮气分压=
×100%=60%,解得x=12,氮气分压=![]() ×60MPa=9MPa;氨气的分压=60%×60MPa=36MPa,氢气分压=60MPa-9MPa-36MPa=15MPa,此时的平衡常数Kp=
×60MPa=9MPa;氨气的分压=60%×60MPa=36MPa,氢气分压=60MPa-9MPa-36MPa=15MPa,此时的平衡常数Kp= =0.043(MPa)-2,故答案为:0.043(MPa)-2。
=0.043(MPa)-2,故答案为:0.043(MPa)-2。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应发生在同种元素之间的是( )
A. Zn+2HCl![]() ZnCl2+H2↑
ZnCl2+H2↑
B. 2H2S+SO2![]() 3S↓+2H2O
3S↓+2H2O
C. H2+CuO![]() Cu+H2O
Cu+H2O
D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组欲设计实验验证Zn、Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制________、________相同;若选用一种盐溶液验证三种金属的活泼性,该试剂________.
(2)①若用Zn、Cu作电极设计成原电池,并能产生持续稳定的电流,以确定Zn、Cu的活动性.试在下面方框中画出原电池装置图,标出原电池的电极材料和电解质溶液_______.

②上述装置中正极反应式为 ________.
③某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用________.
A.0.5molL﹣1氯化亚铁溶液
B.0.5molL﹣1氯化铜溶液
C.0.5molL﹣1盐酸
D.0.5molL﹣1氯化亚铁和0.5molL﹣1氯化铜混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用光洁铂丝蘸取某无色溶液,在无色火焰上灼烧,火焰呈黄色,则无色溶液中
A.只有Na+B.一定有Na+,可能有K+
C.一定有Na+和K+D.可能有Na+和K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下:
弱酸 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)CH3COOH、H2CO3、H2SO3三种酸中酸性最弱的是__________(填化学式)。
(2)CH3COOH的电离平衡常数表达式为K=__________。
(3)写出H2CO3的第二步电离方程式:_____________。
(4)写出H2SO3溶液和CH3COONa溶液反应的离子方程式:____________________。
(5)将体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH的变化如图所示,则HX的电离平衡常数____________(填“大于”“小于”或“等于”)醋酸的电离平衡常数,理由是__________________。
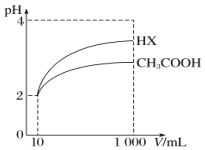
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,已知下列物质燃烧的化学方程式为:
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H=-572kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ.mol-1。
在此条件下,下列叙述正确的是
A. C(s)+2H2(g)=CH4(g) △H=+75.5kJ·mol-1
B. CH4(g)+O2(g)=C(s)+2H2O(g) △H=-1283.5kJ.mol-1
C. 1molH2(g)和3molCH4(g)燃烧共放热2956kJ.mol-1
D. 相同质量的H2和CH4充分燃烧时,H2放出的热量约等于CH4放出的热量的2.57倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物由碳、氢、氧三种元素组成,其红外光谱图只有C—H键、O—H键、C—O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式是
A. CH3CH2OCH3 B. CH3CH(OH)CH3 C. CH3CH2CH2CH2OH D. CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用树状分类法对下列10种物质进行分类
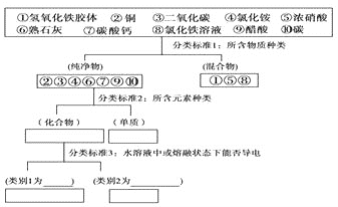
其中,强电解质有:________、弱电解质有:________,写出③的水化物的电离方程式:________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com