
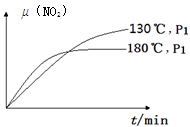
 N2(g)+CO2(g)+2H2O(g) ΔH=?867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=?867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:| 实验编号 | 温度 | 时间 | 0 | 10 | 20 | 40 | 50 |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | | 0.15 |
 4NO(g)+CO2(g)+2H2O(g) ΔH1=?574 kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=?574 kJ·mol-1 2N2(g)+CO2(g)+2H2O(g) ΔH2
2N2(g)+CO2(g)+2H2O(g) ΔH2 N2(g)+CO2(g)+2H2O(g)
N2(g)+CO2(g)+2H2O(g)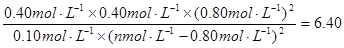 ,解得a=1.2
,解得a=1.2 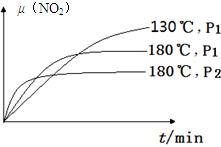
 N2(g)+CO2(g)+2H2O(g)
N2(g)+CO2(g)+2H2O(g) N2(g)+CO2(g)+2H2O(g) ΔH=?867 kJ·mol-1,由于系数加倍焓变也加倍,则2CH4(g)+4NO2(g)
N2(g)+CO2(g)+2H2O(g) ΔH=?867 kJ·mol-1,由于系数加倍焓变也加倍,则2CH4(g)+4NO2(g) 2N2(g)+2CO2(g)+4H2O(g) ΔH=?2×867 kJ·mol-1,由于CH4(g)+4NO2(g)
2N2(g)+2CO2(g)+4H2O(g) ΔH=?2×867 kJ·mol-1,由于CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) ΔH1=?574 kJ·mol-1,根据盖斯定律,前者减去后者可得CH4(g)+4NO(g)
4NO(g)+CO2(g)+2H2O(g) ΔH1=?574 kJ·mol-1,根据盖斯定律,前者减去后者可得CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g),且焓变等于?1160kJ/mol,故ΔH2=?1160kJ/mol。
2N2(g)+CO2(g)+2H2O(g),且焓变等于?1160kJ/mol,故ΔH2=?1160kJ/mol。

科目:高中化学 来源:不详 题型:单选题
A.H2(g)+I2(g)  2HI(g) ΔH<0 2HI(g) ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
C.N2(g)+3H2(g)  2NH3(g)ΔH<0 2NH3(g)ΔH<0 |
D.2SO3(g) 2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
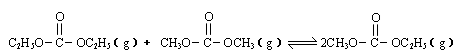 是碳酸甲乙酯的工业生产原理。下图是投料比[
是碳酸甲乙酯的工业生产原理。下图是投料比[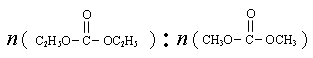 ]分别为3︰1和1︰1、反应物的总物质的量相同时,
]分别为3︰1和1︰1、反应物的总物质的量相同时, 的平衡转化率与温度的关系曲线。下列说法正确的是
的平衡转化率与温度的关系曲线。下列说法正确的是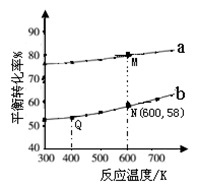
| A.曲线b所对应的投料比为3︰1 |
| B.M点对应的平衡常数小于Q点 |
| C.N点对应的平衡混合气中碳酸甲乙酯的物质的量分数为0.58 |
| D.M点和Q点对应的平衡混合气体的总物质的量之比为2︰1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )
xC(g)ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是 ( )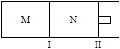
| A.若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) |
| B.若x>3,达到平衡后B的转化率关系为:α(M)>α(N) |
| C.若x<3,C的平衡浓度关系为:c(M)>c(N) |
| D.x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
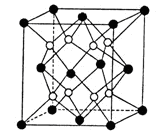
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.该反应的△H>0 |
| B.在提纯过程中,S2的量不断增加 |
| C.该反应的平衡常数与I2的浓度成正比 |
| D.经过足够长时间后,石英管右端将得到纯净的TaS2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题:
C(g)+D(g)达到平衡后,升高温度容器内气体的密度增大。请回答下列问题: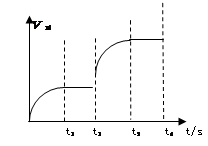
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
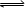
 2C(g) 达到平衡的( )
2C(g) 达到平衡的( )A.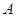 、 、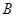 、 、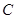 的浓度之比为1:2:2 的浓度之比为1:2:2 |
B.单位时间内消耗 ,同时生成2a mol C ,同时生成2a mol C |
C.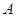 的浓度不再变化 的浓度不再变化 |
| D.混合气体总物质的量为2a mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3 △H=-92.4 kJ·mol-1下图是该反应的速率—时间图像,一定条件下,t1时建立平衡, t2时改变某一条件,t3时又建立新平衡,t2时改变的条件可能是
2NH3 △H=-92.4 kJ·mol-1下图是该反应的速率—时间图像,一定条件下,t1时建立平衡, t2时改变某一条件,t3时又建立新平衡,t2时改变的条件可能是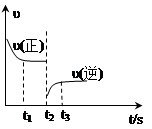
| A.升高温度 | B.分离出部分氨气 |
| C.降低压强 | D.增大反应物浓度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com