
| A. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | |
| B. | CuCl2溶液与NaHS溶液反应,当n(CuCl2):n(NaHS)=1:2时Cu2++2HS-═CuS↓+H2S↑ | |
| C. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,2Fe2++4Br-+3Cl2═2 Fe3++2Br2+6Cl- | |
| D. | Fe与稀硝酸反应,当n(Fe):n(HNO3)=3:8时,3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O |
分析 A.n(OH-):n(Al3+)=3:1时恰好生成沉淀,n(OH-):n(Al3+)=4:1时恰好生成偏铝酸根离子,则n(OH-):n(Al3+)=7:2时生成氢氧化铝和偏铝酸根离子;
B.n(CuCl2):n(NaHS)=1:2时,发生复分解反应生成沉淀和气体;
C.当n(Cl2):n(FeBr2)=1:1时,由电子守恒可知,亚铁离子全部被氧化,溴离子一半被氧化;
D.n(Fe):n(HNO3)=3:8时,由电子守恒可知,生成硝酸亚铁、NO和水.
解答 解:A.n(OH-):n(Al3+)=3:1时恰好生成沉淀,n(OH-):n(Al3+)=4:1时恰好生成偏铝酸根离子,则n(OH-):n(Al3+)=7:2时生成氢氧化铝和偏铝酸根离子,则离子反应为2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O,故A正确;
B.n(CuCl2):n(NaHS)=1:2时,发生复分解反应生成沉淀和气体,离子反应为Cu2++2HS-═CuS↓+H2S↑,故B正确;
C.当n(Cl2):n(FeBr2)=1:1时,由电子守恒可知,亚铁离子全部被氧化,溴离子一半被氧化,离子反应为2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-,故C错误;
D.n(Fe):n(HNO3)=3:8时,由电子守恒可知,生成硝酸亚铁、NO和水,离子反应为3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O,故D正确;
故选C.
点评 本题考查离子反应方程式的书写的正误判断,为高频考点,把握发生的反应及离子反应方程式的书写方法为解答的关键,侧重与量有关的离子反应、复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


科目:高中化学 来源: 题型:解答题
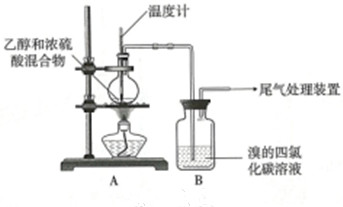
| 操作 | 现象 |
| 点燃酒精灯, 加热至170℃ | a.A中烧瓶内液体渐渐变黑 b.B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕 | c.A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏的方法分离水和油的混合物 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量泥沙 | |
| C. | 用分液的方法分离酒精和水的混合物 | |
| D. | 用加热、蒸发的方法可以除去NaCl中CaCl2、MgCl2等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3比NaHCO3易溶于水 | B. | Na2CO3比NaHCO3稳定 | ||
| C. | Na2CO3和NaHCO3都能与盐酸反应 | D. | Na2CO3俗名:小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定不存在的离子是Mg2+、Ba2+,不能确定是否含有K+、NO3- | |
| B. | 一定存在的离子是CO32-、SO42-,CO32-的物质的量浓度为0.25mol•L-1,SO42-的物质的量浓度为0.1mol•L-1 | |
| C. | 一定存在的离子是CO32-、SO42-、K+,其中K+浓度≥0.2mol•L-1 | |
| D. | 一定存在的离子是CO32-、SO42-、K+,其中K+浓度为0.2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Al3+、SO42-、HCO3- | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | Fe3+、Mg2+、SO42-、NO3- | D. | Cu2+、K+、NO3-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
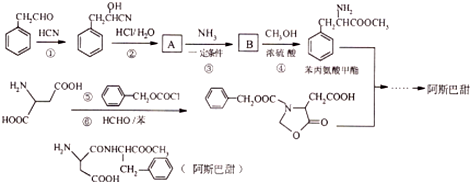
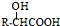 $→_{一定条件}^{NH_{3}}$
$→_{一定条件}^{NH_{3}}$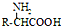
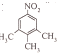 、
、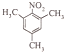 ;
;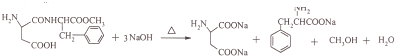 ;
;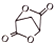 的合成路线流程(无机试剂任选).合成路线流程示例如下 CH2═CH3$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$ CH3CH2OH:
的合成路线流程(无机试剂任选).合成路线流程示例如下 CH2═CH3$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$ CH3CH2OH: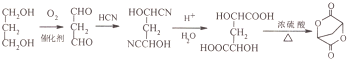 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用广泛pH试纸测得 0.1mol/L NH4Cl溶液的pH=5.2 | |
| B. | 酸碱中和滴定时锥形瓶用蒸馏水洗涤后,再用待测液润洗后装液进行滴定 | |
| C. | 将碘水倒入分液漏斗,加入适量苯振荡后静置,从分液漏斗下口放出碘的苯溶液 | |
| D. | 常温常压下,将15g NO和8g O2混合,所得混合气体分子总数小于0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com