
����Ŀ���ݱ������������ѧ��ʹ����ͨ�����Ӻʹ���������������ã����������͵�������O4�����Ľṹ�ܸ��ӣ����ܾ�����S4���Ƶij����νṹ����һ�ָ��������ӡ�
�������й�˵���У�����ȷ����________������ĸ����
A��O4�����ڴ��ڹ��ۼ�
B���ϳ�O4�ķ�Ӧ�ɿ����˾۱䷴Ӧ���������ڻ�ѧ�仯
C��O4��O3��O2������Ԫ�ص�ͬ������
D��O4������������ǿ�����Ļ���ƽ���������
���Ʊ�O2����O22������O22+�Ļ������ǿ��ܵģ�ͨ���������������ӽ�����ͼ��ʾ�ĸ��ַ�Ӧʱ���ɡ���Щ��Ӧ�У��൱�������ӵ���������_______������ţ����൱�������ӵĻ�ԭ����_______������ţ���

��O22+����ԭ�Ӽ��γ�3�Թ��õ��Ӷ�ʹ��ԭ�Ӵﵽ�ȶ��ṹ��д��O22+�ĵ���ʽ______��
���𰸡�AB �� �٢� ![]()
��������
��1��A.����ͬ�ǽ���Ԫ�ص�ԭ��֮�䲻���γɼ��Թ��ۼ��жϣ�
B.�ϳ�O4�ķ�Ӧ��Ԫ������䣬���ڻ�ѧ�仯��
C.��ͬ��Ԫ����ɵIJ�ͬ���ʣ�����ͬ�������壻
D.�Ա�O3��O2�����ʣ�O4�������Ը�ǿ��
��2��Ԫ�ػ��ϼ����ߣ���������Ԫ�ػ��ϼ۽��ͣ�����ԭ��
��3��O22+�ĵ���ʽΪ��![]() ��
��
��1��A.ͬ�ǽ���Ԫ�ص�ԭ��֮��ֻ���γɷǼ��Թ��ۼ�����A����
B.�ϳ�O4�ķ�Ӧ��Ԫ������䣬���ڻ�ѧ�仯����B����
C.O4��O3��O2������Ԫ����ɵIJ�ͬ���ʣ�����ͬ�������壬��C��ȷ��
D.�Ա�O3��O2�����ʣ�O4�������Ը�ǿ����������ǿ�����Ļ���ƽ�������������D��ȷ��
�ʴ�Ϊ��AB��
��2���������Ʊ���O22+�ı仯�У�Ԫ�ػ��ϼ����ߣ��൱�������ӱ������� �Ʊ���O2����O22���ı仯�У�Ԫ�ػ��ϼ۽��ͣ��൱�������ӱ���ԭ���ʴ�Ϊ�������٢���
��3��O22+����ԭ�Ӽ��γ�3�Թ��õ��Ӷ�ʹ��ԭ�Ӵﵽ�ȶ��ṹ��������ʽΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ��H=��190kJ/mol������˵����ȷ����
O2(g)=CO2(g)+2H2(g) ��H=��190kJ/mol������˵����ȷ����
A.CH3OH��ȼ����Ϊ190kJ/mol
B.�÷�Ӧ˵��CH3OH��H2�ȶ�
C.��Ӧ�е������仯�뷴Ӧ��ϵ���¶Ⱥ�ѹǿ��
D.CO2(g)+2H2(g)=CH3OH(g)+![]() O2(g) ��H=+190kJ/mol
O2(g) ��H=+190kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��KClO3��6HCl��KCl��3Cl2����3H2O�����н�����ȷ����
A.�����ԣ�Cl2��KClO3
B.HCl����ԭ����ȫ��������
C.KClO3 ��������������������
D.����3 mol Cl2 ��ת�Ƶ��ӵ����ʵ���Ϊ6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����ڿ��淴ӦX(g)��3Y(g) ![]() 2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊ c1��c2��c3(����Ϊ��)���ﵽƽ��ʱX��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol��L-1��0.3 mol��L-1��0.08 mol��L-1���������ж���ȷ����
2Z(g)����X��Y��Z����ʼŨ�ȷֱ�Ϊ c1��c2��c3(����Ϊ��)���ﵽƽ��ʱX��Y��Z��Ũ�ȷֱ�Ϊ0.1 mol��L-1��0.3 mol��L-1��0.08 mol��L-1���������ж���ȷ����
A. c1��c2��3��1B. ƽ��ʱ��Y��Z����������֮��Ϊ2��3
C. X��Y��ת�������D. c1��ȡֵ��ΧΪ0.04 mol��L-1 < c1 < 0.14 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������п������̼������Ϊ������ϣ�����������ԭ��ӦH2SO4+Zn��ZnSO4+H2�����������ԭ���װ�ã�
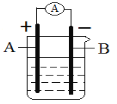
�Ÿ�ԭ��ص������Һ�е�������________��
�Ƶ缫A��________���õ缫��Ӧ����Ϊ_______��
�ǵ缫B��______���õ缫��Ӧ����Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������![]() ��һ����Ҫ�Ļ�ѧ�Լ���ij��ȤС���ڿα��ϳɷ����Ļ����Ͻ����˸Ľ����������£�
��һ����Ҫ�Ļ�ѧ�Լ���ij��ȤС���ڿα��ϳɷ����Ļ����Ͻ����˸Ľ����������£�

��1������˵����ȷ����_________��
A������м����![]() ��Һ��ȥ��������ۣ�ͨ�����ó��˳�ȥ��Һ
��Һ��ȥ��������ۣ�ͨ�����ó��˳�ȥ��Һ
B��ʵ����ʹ�õ�����ˮ������г���
C���ڼ��������ǰ��Ӧ�ð�����������Һ��pHֵ������ǿ���Է�Χ��
D���������þ����к���![]() ������ȡ������Ʒ���Թ��У���ˮ�ܽ⣬����NaOH��Һ��¶���ڿ����У��۲�����
������ȡ������Ʒ���Թ��У���ˮ�ܽ⣬����NaOH��Һ��¶���ڿ����У��۲�����

��2������м����̼��������ʣ�Ϊ�Ͽ���Ƶýϴ�����![]() ������ȤС�����ͼ��װ�����Ʊ���Ʒ����ѡ���������Լ��е�һ���������ʵ�顣
������ȤС�����ͼ��װ�����Ʊ���Ʒ����ѡ���������Լ��е�һ���������ʵ�顣
a.![]() ��Һ b.̼�� c.
��Һ b.̼�� c.![]() ��Һ e.
��Һ e.![]() ��Һ f.�Ҵ�
��Һ f.�Ҵ�
����ȥ���ۺ�ķ���м�м���һ�����ʣ������ʿ���Ϊ_________��
����ϴ��ƿ��װ��һ�����ʣ������ʿ���Ϊ_________��
��3�������ľ��������Ѹ��ȡ��Һ���������У������ڻ������������Ҵ���ʹ֮������Һ���ϣ������Ҵ�����Һ�в�����ɢ������������ᾧ�������÷������ŵ��ǣ�д���������㣩_________��
��4���Ƶ�![]() ����Ҫ�Ծ�����и���α��øɾ�����ֽ���ɣ�����ȤС��ͬѧ�������ۣ������ü�ѹ���װ����ͼ����ʾ������Ʒ�������������ˮ�ó��������Ʋ������ɡ��������������ǰ������__________________��Ȼ�����ǡ�
����Ҫ�Ծ�����и���α��øɾ�����ֽ���ɣ�����ȤС��ͬѧ�������ۣ������ü�ѹ���װ����ͼ����ʾ������Ʒ�������������ˮ�ó��������Ʋ������ɡ��������������ǰ������__________________��Ȼ�����ǡ�
��5����Ʒ���������IJⶨ���Բ������Ը�����صζ��ķ�����������ر���Һ���������ȶ���Ħ�������ϴ�Ļ����ʲ����ƽ��б궨����Ӧԭ��Ϊ��
![]() ��
��
ʵ�鲽�����£�
����һ���ȴ���Ũ��ԼΪ![]() �ĸ��������Һ250mL��
�ĸ��������Һ250mL��
���������ȡ�����ƹ���m g������ƿ�У���������ˮ�ܽⲢ�������ữ�����ȵ�![]() ��������
��������![]() �ζ����Ӷ��궨
�ζ����Ӷ��궨![]() Ũ��Ϊ
Ũ��Ϊ![]() ��
��
����������ȡ��Ʒ2��031g��������ƿ��������ˮ�ܽ⣻
�����ģ��ñ�![]() ��Һ�ζ�������������Ʒ��Һ���ﵽ�յ�ʱ���ı�Һ45��00mL��
��Һ�ζ�������������Ʒ��Һ���ﵽ�յ�ʱ���ı�Һ45��00mL��
�ٲ���һ��������Ҫ�õ��IJ����������ձ���___________��___________��
�ڲ��������Ҫ��m��ֵ����Ԥ�������Ԥ��������____________��
a.��������������Ũ�� b.��Ӧ�Ķ�����ϵ
c.�ζ��ܵ�������� d.�����ܽ�����Ƶ�ˮ�����
��ʵ���������Ҫ���ж�εζ����ڵζ�����ǰҪ����һϵ�в�������ѡ����ʵı�ţ�����ȷ��˳������____________��
a.����ʽ�ζ����м�װ�����Һ����0���̶����ϣ�
b.������ˮϴ�ӵζ��ܣ�
c.���ζ�����װ��ˮ��ֱ���ڵζ��ܼ���Լ2min��
d.�ò�����Һ��ϴ�ζ��ܣ�
e.��������ת![]() ���ٴι۲죻
���ٴι۲죻
f.���ζ���ֱ���ڵζ��ܼ��ϣ����â�������ң�������
g.������ס�ζ���ʹ����б![]() ������Ѹ�ٴ�����
������Ѹ�ٴ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ͨ�����з�Ӧ��ʵ��ȼú��������Ļ��գ�SO2(g)��2CO(g)![]() 2CO2(g)��S(l)����H��0����Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ����
2CO2(g)��S(l)����H��0����Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ����
A. ƽ��ǰ�����ŷ�Ӧ�Ľ��У�������ѹǿʼ�ղ���
B. ƽ��ʱ�������������䣬�����������Ӧ���ʼӿ�
C. ƽ��ʱ�������������䣬�����¶ȿ����SO2��ת����
D. �����������䣬ʹ�ò�ͬ�������÷�Ӧ��ƽ�ⲻ�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڻ�ѧ��Ӧ�У���������ѧ��Ӧ�ķ��Ӽ���ײ��֮Ϊ��Ч��ײ����Щ���ӳ�Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ����������л�ܣ��䵥λ��kJmol-1��ʾ��������۲���ͼ��Ȼ��ش����⡣

��1��ͼ�з�Ӧ��______��������������������������Ӧ���÷�Ӧ_______��������Ҫ����������Ҫ�����������ṩ�������÷�Ӧ����H=_________���ú�E1��E2�Ĵ���ʽ��ʾ����
��2����֪�Ȼ�ѧ����ʽ��H2(g)+1/2O2(g) =H2O(g) ��H= ��241.8kJmol-1���÷�Ӧ�Ļ��Ϊ167.2 kJmol-1�������淴Ӧ�Ļ��Ϊ__________��
��3������ͬһ��Ӧ��ͼ������(��)��ʵ��(I)��ȣ����_________����λ����ڻ���ӵİٷ���________����˷�Ӧ����_________����ǰ�����������������������С����������������Ϊ����ܵ�ԭ����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.�����Ǽ���ʵ���г��õ�������
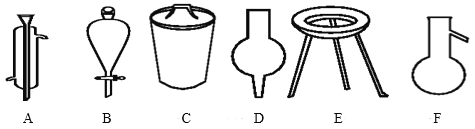
д����������������������ƣ�
A__��B__��C__��D___��E___F___��
��.ʵ����Ҫ����100mL1mol/LNaCl��Һ����ش��������⣺
��1�����ƹ�������Ҫʹ�õ���Ҫ�������������ձ�������������ͷ�ιܡ���ƽ����Ͳ��___��
��2����������ƽ��ȡ�Ȼ��ƹ��壬������Ϊ___g��
��3��������Ҫ�����������ȷ˳����___(�����)��
�ٳ�ȡһ���������Ȼ��ƣ������ձ��У�����������ˮ�ܽ⣻
�ڼ�ˮ��Һ��������ƿ���̶�����1��2����ʱ�����ý�ͷ�ιܵμ�����ˮ����Һ����̶������У�
�۽���Һת�Ƶ�����ƿ�У�
�ܸǺ�ƿ�����������µߵ� ��ҡ�ȣ�
������������ˮϴ���ձ��ڱںͲ�����2��3�� ��ϴ��Һת�Ƶ�����ƿ�С�
��4�����ʵ�������ȱ�ٲ���ݣ������������Һ�����ʵ���Ũ��___(����ƫ��"����ƫ��"������Ӱ����)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com