
已知元素周期表中共有18纵行,如图实线表示元素周期表的边界,按电子排布,可把周期表划分为s区、p区、d区、ds区等。除ds区外,其他区的名称均按构造原理最后填入电子的能级符号来命名。
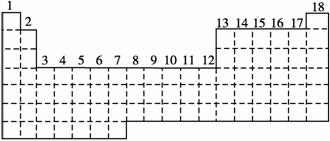
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区。
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另
一区,你认为应排在________区。
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:______________。
(5)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元
素周期表共可以排布________种元素。
解析 29号元素原子的价电子排布,理论上也可以排成3d94s2,但实际上却
排成3d104s1,这是由能量最低原理决定的,即轨道处于全空、半充满或全充
满时,轨道能量最低。相比之下,第6、7纵行和第11纵行与其类似,当第6、
7纵行元素原子的价电子处于半充满状态时,轨道能量最低,所以可将第6、7
纵行部分元素排在ds区。
答案 (1)
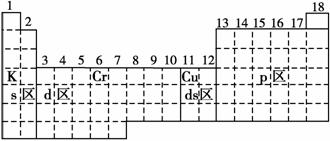
(2)ds
(3)如上图所示
(4)Fe原子的价电子排布式为3d64s2,Fe2+为3d6,Fe3+为3d5;依据“能量相
同的轨道处于全空、全充满或半充满时能量最低”的原则,Fe3+的3d轨道处
于半充满状态,结构比Fe2+的稳定,故Fe3+比Fe2+稳定 (5)118


科目:高中化学 来源: 题型:
有关天然产物水解的叙述不正确的是( )
A.油脂水解可得到丙三醇
B.可用碘检验淀粉水解是否完全
C.蛋白质水解的最终产物均为氨基酸
D.纤维素水解与淀粉水解得到的最终产物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
为了合理利用化学能确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,5 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,试写出甲醇燃烧的热化学方程式:___________________________________________。
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2(g)+3H2(g)2NH3(g) ΔH=a kJ·mol-1。试根据表中所列键能数据估算a的数值:
________________________________________________________________________。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:
C(石墨,s)+O2(g)===CO2(g)
ΔH1=-393.5 kJ·mol-1①
2H2(g)+O2(g)===2H2O(l)
ΔH2=-571.6 kJ·mol-1②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)
ΔH3=-2 599 kJ·mol-1③
根据盖斯定律,计算298 K时由C(石墨,s)和H2(g)生成1 mol C2H2(g)反应的焓变:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )。
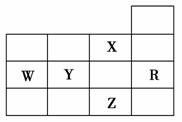 A.W元素的第一电离能小于Y元素的第一电离
A.W元素的第一电离能小于Y元素的第一电离
能
B.Y、Z的阴离子电子层结构都与R原子的相同
C.p能级未成对电子最多的是Z元素
D.X元素是电负性最大的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
( )。
A.乙烯的结构简式可以表示为CH2CH2
B.苯、乙醇和乙酸都能发生取代反应
C.油脂都不能使溴的四氯化碳溶液褪色
D.液化石油气和天然气的主要成分都是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等明显药效的健康食品。苹果酸(2羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为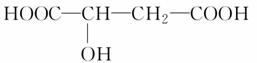 。下列相关说法不正确的是
。下列相关说法不正确的是
( )。
A.苹果酸在一定条件下能发生酯化反应
B.苹果酸在一定条件下能发生催化氧化反应
C.1 mol苹果酸与足量Na反应生成33.6 L H2(标准状况下)
D.1 mol苹果酸与Na2CO3溶液反应一定消耗2 mol Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是
( )。
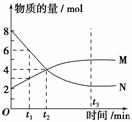
A.化学方程式为:2M
 N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式不正确的是( )
A.Na2CO3溶液与足量盐酸反应:CO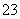 +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
B.FeCl2溶液和Cl2反应:2Fe2++Cl2===2Fe3++2Cl-
C.钠与水反应:Na+H2O===Na++OH-+H2↑
D.NaHCO3溶液与稀硝酸反应:HCO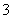 +H+===CO2↑+H2O
+H+===CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com