
在20mL 0.0025mol·L-1 AgNO3溶液中,加入5mL 0.01mol·L-1 KCl溶液,通过计算判断是否有AgCl沉淀生成。已知Ksp(AgCl)=1.8×10-10 (混合后溶液的总体积为两者体积之和)。
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
下列是关于物质结构中微粒的常见关系,正确的是
A.在含4 mol Si—O键的二氧化硅晶体中,氧原子的数目为4NA
B.金刚石晶体中,碳原子数与六碳环数之比为2∶1
C.石墨晶体中,六碳环数与碳碳键数之比为2∶3
D.氯化钠晶体中,钠离子和氯离子的配位数都为8
查看答案和解析>>
科目:高中化学 来源: 题型:
Cu(OH)2在水溶液中存在着如下沉淀溶解平衡:Cu(OH)2(s)  Cu2+(aq)+2OH-(aq),在常温下Ksp=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol/L的CuSO4溶液中加入碱来调整溶液的pH,应使溶液的pH大于( )
Cu2+(aq)+2OH-(aq),在常温下Ksp=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol/L的CuSO4溶液中加入碱来调整溶液的pH,应使溶液的pH大于( )
A.2 B.3 C.4 D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是 。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是 。
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是 。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是 。
(5)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为 ,反应所需时间的长短关系是 。
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用图中所示实验装置证明氧化铜能加快约7%的双氧水的分解并与二氧化锰的催化效果进行比较(即比较反应速率)。用图示装置测量产生气体的体积,其他可能影响实验的因素均已忽略,相关数据如下:
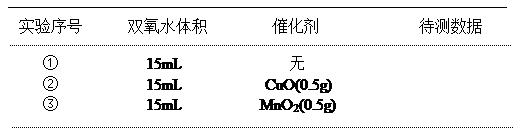
(1)从实验原理来看,实验中的“待测数据”可以指 、也可以指 。
(2)实验时气体收集在B中,B仪器名称是__________。若要检验产生的气体是O2,待气体收集结束后,用弹簧夹夹住B下端乳胶管,打开单孔橡皮塞, 。

(3)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验不必写具体步骤):a.证明CuO的化学性质没有变化,b. 。
(4)为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是 。
(5)实验开始时,当往容器中加入一定量的双氧水后,由于短时间内产生大量气体,分液漏斗内的液体不能顺利流下,为了解决这个问题,你采取的措施是 ;
在测量生成的气体体积时,除了要注意视线与凹液面相平以外,还应注意
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同
B.某金属阳离子的结构示意图为:
其与Cl-形成的强电解质都是离子化合物
C.二硫化碳是直线形非极性分子,其电子式为:

D.中子数为18的氯原子可表示为18Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.已知甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.常温下反应C(s)+CO2(g)=2CO(g)不能自发进行是由于该反应△H>0
C.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.已知2NaOH(aq)+H2SO4(aq) = Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ/mol,则该反应的中和热为114.6 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com