
 和
和
 和
和

分析 根据结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;分子式相同,结构不同的化合物互称为同分异构体;质子数相同中子数不同的原子互称同位素;同种元素形成的不同单质互为同素异形体;同种物质指组成和结构都相同的物质;然后对照概念分析.
解答 解:①O2和O3均是氧元素形成的不同种单质,互称为同素异形体;
②苯和甲苯,结构相似,在分子组成上相差一个CH2原子团,互称为同系物;
③ 和
和 相当于甲烷的四个H分别被2个Cl和2个F取代,甲烷为正四面体结构,故两者是一种物质;
相当于甲烷的四个H分别被2个Cl和2个F取代,甲烷为正四面体结构,故两者是一种物质;
④CH3CH3和CH3CH2CH2CH3结构相似,在分子组成上相差2个CH2原子团,互称为同系物;
⑤金刚石和石墨均是碳元素形成的不同种单质,互为同素异形体;
⑥ 和
和 分子式不同,结构不同,不属于同系物,也不属于同分异构体;
分子式不同,结构不同,不属于同系物,也不属于同分异构体;
⑦CH3CH2NO2和 分子式相同,结构不同,属于同分异构体;
分子式相同,结构不同,属于同分异构体;
⑧氕、氘和氚 均属于氢元素的不同种原子,互为同位素;
⑨CH3CH2CH(CH3)CH(CH3)CH3和CH3CH(CH3)CH(CH3)3分子式相同,结构不同,属于同分异构体,
(1)互为同系物的是②④,故答案为:②④;
(2)互为同分异构体的是⑦⑨,故答案为:⑦⑨;
(3)属于同位素的是⑧,故答案为:⑧;
(4)互为同素异形体的是①⑤,故答案为:①⑤;
(5)属于同一种物质的是③,故答案为:③.
点评 本题主要考查了同系物、同分异构体、同位素、同素异形体、同一物质的区别,难度不大,注意把握概念的内涵与外延.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2,O3 | B. | ${\;}_{6}^{13}$C,${\;}_{6}^{12}$C | C. | 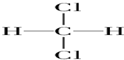 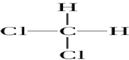 | D. | CH3CH3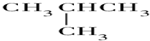 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molD(氘)的质量与NA个T(氚)的质量相等 | |
| B. | NA个氧分子和NA个氢分子的质量比为16:1 | |
| C. | 28g氮气所含原子数目为2NA | |
| D. | 在标准状况下,0.5NA个氯气分子所占的体积约是11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷是共价化合物 | B. | 甲烷分子具有正四面体结构 | ||
| C. | 甲烷分子具有极性键 | D. | 甲烷分子中H-C-H的键角为90℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 混合物 | 需加入的试剂 | 分离方法 |
| 苯(苯酚) | ||
| 乙烷(乙烯) | c | C |
| 乙醇(水) | e | |
| 乙酸乙酯(乙酸) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
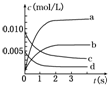 在2L密闭容器内,800℃时反应2SO2(g)+O2(g)=2SO3(g)体系中,n(SO2)随时间的变化如下表:
在2L密闭容器内,800℃时反应2SO2(g)+O2(g)=2SO3(g)体系中,n(SO2)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com