
分析 (1)根据配制的是浓度约为0.1mol•L-1的NaOH溶液来判断;
(2)NaOH在空气中极易吸水,导致NaOH的真实的质量偏小,来分析浓度;
(3)根据醋酸含量约为6g/100mL,计算出醋酸的物质的量,然后根据c=$\frac{n}{V}$来计算;酸碱中和滴定中待测液的浓度要为0.1mol/L左右;
(4)根据稀释醋酸的操作来分析需要的仪器;
(5)根据加入的指示剂是酚酞来分析滴定终点;
(6)根据达滴定终点时,n(CH3COOH)=n(NaOH)来计算.
解答 解:(1)由于配制的是浓度约为0.1mol•L-1的NaOH溶液,是比较粗略的配制,故该配制步骤是可行的,故答案为:可行;
(2)NaOH在空气中极易吸水,导致NaOH的真实的质量偏小,则配制出的溶液的浓度偏小,故答案为:小;
(3)根据醋酸含量约为6g/100mL,则醋酸的物质的量n=$\frac{m}{M}$=$\frac{6g}{60g/mol}$=0.1mol,醋酸的物质的量浓度c=$\frac{n}{V}$=$\frac{0.1mol}{0.1L}$=1mol/L;酸碱中和滴定中待测液的浓度要为0.1mol/L左右,故滴定前要将醋酸溶液稀释10倍,故答案为:1;10;
(4)稀释醋酸的操作需要的仪器有烧杯、玻璃棒、滴管、酸式滴定管、容量瓶,故答案为:容量瓶;
(5)由于是用碱滴定酸,指示剂是酚酞,故当溶液变成浅红色且30秒内不褪色时达到滴定终点,故答案为:溶液变成浅红色且30秒内不褪色;
(6)设原白醋中醋酸的物质的量浓度为Xmol/L,根据达滴定终点时,n(CH3COOH)=n(NaOH),可有$\frac{xmol/L}{10}$×0.02L=c mol•L-1×Vml×10-3,解得x=$\frac{CV}{2}$mol/L,
故答案为:$\frac{CV}{2}$.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:解答题
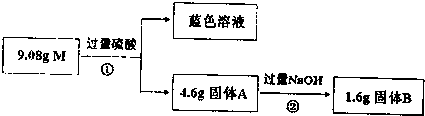
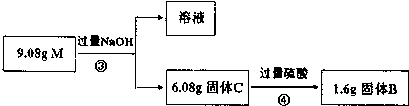
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
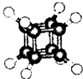
| A. | 它的一氯代物只有一种同分异构体 | |
| B. | 它的二氯代物有三种同分异构体 | |
| C. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 | |
| D. | 它是一种不饱和烃,既能发生取代反应,又能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
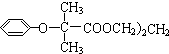
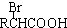 $\stackrel{苯酚钠}{→}$
$\stackrel{苯酚钠}{→}$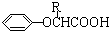
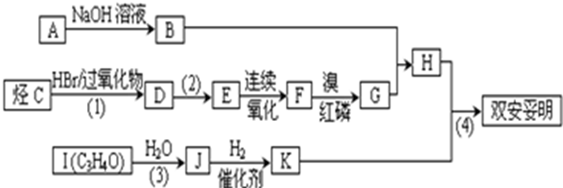

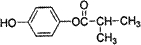 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为9NA | |
| B. | 42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA | |
| C. | 标准状况下,11.2L苯中含有的碳碳双键数为1.5NA | |
| D. | 5.6g铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 360 | 440 | 520 |
| K | 0.036 | 0.010 | 0.0038 |
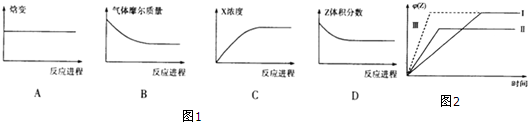
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 打开盛装NO的集气瓶;冷却NO2气体 | |
| B. | 用冰水混合物冷却SO3气体;加热氯化铵晶体 | |
| C. | 木炭吸附NO2气体;将氯气通入品红溶液中 | |
| D. | 向酚酞溶液中加入Na2O2;向FeCl3溶液中滴加KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它处在元素周期表中第二周期ⅤA族 | |
| B. | 它的最高正价为+5,负价为-3 | |
| C. | 它的最高价氧化物对应水化物是一元强酸 | |
| D. | 它的非金属性比磷弱比氧强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com