
| A. | 元素电负性越大的原子,吸引电子的能力越强 | |
| B. | 在NH4+ 和[Cu(NH3)4]2+中都存在配位键 | |
| C. | SO2、SO3都是极性分子 | |
| D. | NF3较NH3难于与Cu2+形成配位键 |
分析 A.元素电负性是表示对键合电子的吸引力的大小;
B.NH4+中N原子与H+形成配位键,[Cu(NH3)4]2+中Cu2+与NH3之间的化学键为配位键;
C.SO2是极性分子,SO3分子是非极性分子;
D.F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤电子对的吸引能力增强,难以形成配位键.
解答 解:A.非金属性越强,电负性越大,该元素的原子吸引电子的能力越强,故A正确;
B.NH4+中N原子与H+形成配位键,[Cu(NH3)4]2+中Cu2+与NH3之间形成配位键,所以在NH4+ 和[Cu(NH3)4]2+中都存在配位键,故B正确;
C.SO2是极性分子,SO3分子是非极性分子,所以二者分子的极性不同,故C错误;
D.F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤电子对的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子,故D正确;
故选C.
点评 本题考查了分子极性的判断、配位键、电负性,题目考查知识点较多,但是较基础,难度不大,侧重于考查学生对基础知识的应用能力.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 序号 | ① | ② | ③ | ④ | ③ | ⑥ |
| 仪器及装置图 | 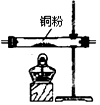 |  |  |  | 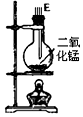 |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 稀硫酸与Ba(OH)2溶液混合:SO42-+Ba2+═BaSO4↓ | |
| C. | 稀硝酸滴在大理石上:CaCO3+2H+═Ca2++H2CO3 | |
| D. | 氧化铁与稀盐酸混合:Fe2O3+6H+═2Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 溶质所含离子 | SO42- | M | Mg2+ | Fe2+ |
| 物质的量浓度 | c | 3 | 3 | 2 |
| A. | 若M是NO3-,则c为3.5 | |
| B. | 若使Fe2+浓度降低,可以加入试剂NaOH | |
| C. | 若M是NH4+,则配制溶液所用的溶质不一定是3种 | |
| D. | 若加入BaCl2溶液能产生两种沉淀,则M可能是CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能全部透过半透膜 | B. | 所得物质一定为悬浊液或乳浊液 | ||
| C. | 所得混合物一定能导电 | D. | 有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
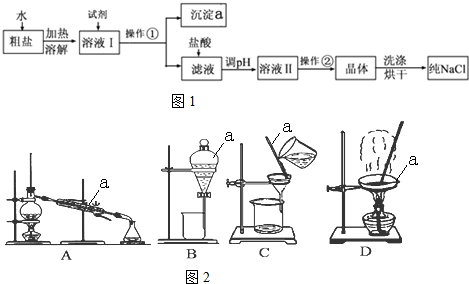
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解 | |
| B. | 滤去不溶性杂质后,将滤液移至坩埚内加热浓缩 | |
| C. | 将制得的晶体转移到新制过滤器中用大量水进行洗涤 | |
| D. | 当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com