
| A. | 增大H2O2的浓度 | B. | 加入少量MnO2粉末 | ||
| C. | 加入几滴FeCl3溶液 | D. | 把盛有H2O2溶液的试管放在冰水里 |
分析 增大反应物浓度、增大反应物接触面积、升高温度、加入催化剂等都影响反应速率,该反应中要增大反应速率,可以采用增大反应物浓度、加入催化剂、升高温度等方法,据此分析解答.
解答 解:A.增大双氧水浓度,增大单位体积内活化分子个数,所以反应速率增大,故A不选;
B.加入少量二氧化锰粉末,增大活化分子百分数,所以反应速率增大,故B不选;
C.加入几滴氯化铁溶液,增大活化分子百分数,反应速率增大,故C不选;
D.把盛有H2O2溶液的试管放在冰水里,温度降低,减少活化分子百分数,反应速率减小,故D选;
故选D.
点评 本题考查化学反应速率影响因素,为高频考点,明确浓度、温度、催化剂对反应速率影响原理是解本题关键,注意该反应中氯化铁能作催化剂,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 2.4gMg和6.5g Zn | B. | Mg和Zn各2.5g | C. | Mg和Al各2.5g | D. | 2.3gNa和2.4gMg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7种和2种 | B. | 8种和3种 | C. | 42种和3种 | D. | 56种和3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是还原剂 | B. | C被氧化 | ||
| C. | SiO2发生氧化反应 | D. | O得到电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
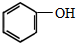 (制酚醛树脂)
(制酚醛树脂) 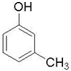 (生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料) ⑥HCHO( 防腐剂 )
(生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料) ⑥HCHO( 防腐剂 )查看答案和解析>>
科目:高中化学 来源: 题型:解答题
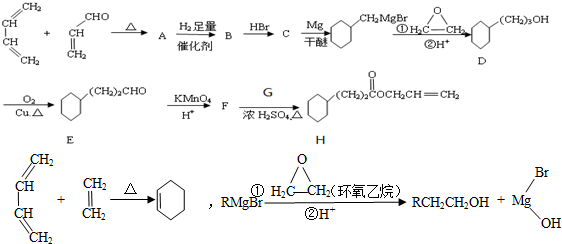
 ,G物质核磁共振氢谱共有4个峰.
,G物质核磁共振氢谱共有4个峰. .写出D生成E的化学方程式
.写出D生成E的化学方程式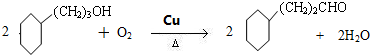 .
.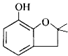 呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式:
呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式: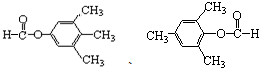 .
.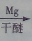 CH3CH2MgBr
CH3CH2MgBr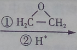 CH3CH2CH2CH2OH.
CH3CH2CH2CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (NH4)2CO3+H2SO4═(NH4)2SO4+H2O+CO2↑ | |
| B. | NaHCO3+HNO3═NaNO3+H2O+CO2↑ | |
| C. | Na2CO3+2CH3COOH═2CH3COONa+H2O+CO2↑ | |
| D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
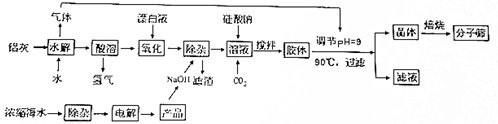
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com