
| A. |  含0.01 mol NaOH和0.01 mol Ba(OH)2的混合溶液中缓慢通入CO2 | |
| B. |  KHCO3溶液中逐滴加入Ba(OH)2溶液 | |
| C. |  KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 | |
| D. |  向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸 |
分析 A.发生的反应为:Ba(OH)2+CO2=BaCO3↓+H2O、2NaOH+CO2=Na2CO3+H2O、Na2CO3+CO2+H2O=2NaHCO3、BaCO3+CO2+H2O=Ba(HCO3)2,当Na2CO3完全反应后,碳酸钡再和二氧化碳反应;
B.KHCO3溶液中逐滴加入Ba(OH)2溶液,发生反应为Ba(OH)2+KHCO3=BaCO3↓+KOH+H2O;
C.向硫酸铝钾中滴入氢氧化钡溶液时发生的离子方程式有Ba2++SO42-═BaSO4↓、Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,根据物质间的反应判断;
D.先发生NaOH与盐酸的反应不生成沉淀,然后发生NaAlO2+HCl+H2O=Al(OH)3↓+NaCl、Al(OH)3+3HCl=AlCl3+3H2O,根据方程式确定产生沉淀与沉淀消失阶段消耗盐酸的体积.
解答 解:A.发生的反应为:Ba(OH)2+CO2=BaCO3↓+H2O、2NaOH+CO2=Na2CO3+H2O、Na2CO3+CO2+H2O=2NaHCO3、BaCO3+CO2+H2O=Ba(HCO3)2,当Na2CO3完全反应后,碳酸钡再和二氧化碳反应,所以生成碳酸钡、氢氧化钠反应生成碳酸氢钠、消失碳酸钡需要二氧化碳的物质的量之比为1:1:1,所以其图象应该是 ,故A错误;
,故A错误;
B.KHCO3溶液中逐滴加入Ba(OH)2溶液,发生反应为Ba(OH)2+KHCO3=BaCO3↓+KOH+H2O,所以图象与实际相符,故B正确;
C.向硫酸铝钾中滴入氢氧化钡溶液时发生的离子方程式有Ba2++SO42-═BaSO4↓、Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,
假设n(KAl(SO4)2)=2mol,当n(Ba(OH)2)≤3mol,发生的反应为Ba2++SO42-═BaSO4↓、Al3++3OH-═Al(OH)3↓,沉淀的质量为m(BaSO4)+m(Al(OH)3),铝离子完全沉淀时,还剩n(SO42-)=1mol;
当3mol<n(Ba(OH)2)≤4mol,发生的反应为Ba2++SO42-═BaSO4、Al(OH)3+OH-═AlO2-+2H2O,沉淀的质量为硫酸钡减去溶解的氢氧化铝的质量,硫酸根离子完全沉淀时,铝元素完全转化为偏铝酸根离子,生成的n(BaSO4),溶解的n(Al(OH)3)=2mol,固体增加质量=233g/mol×1mol-78g/mol×2mol=77g>0,再继续加入氢氧化钡溶液,固体的质量不变,所以其图象为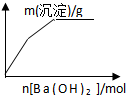 ,故C错误;
,故C错误;
D.先发生NaOH与盐酸的反应不生成沉淀,然后发生NaAlO2+HCl+H2O=Al(OH)3↓+NaCl、Al(OH)3+3HCl=AlCl3+3H2O,沉淀生成与溶解消耗酸为1:3,图象与实际不符,故D错误;
故选B.
点评 本题考查了图象分析,明确物质间的反应及物质的性质是解本题关键,根据物质之间量的关系进行解答,难点是根据其分界点确定发生的反应,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅熔点高硬度大,可用于制作半导体材料 | |
| B. | 氢氧化铝胶体具有吸附性,可用于制胃酸中和剂 | |
| C. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| D. | 氧化铁呈红棕色,可用于制作红色涂料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、HBr、HI稳定性逐渐减弱 | |
| B. | 单质F2、Cl2、Br2、I2中,与氢气化合最容易的是F2 | |
| C. | HF、HCl、HBr、HI中酸性最强的是HF | |
| D. | 单质F2、Cl2、Br2、I2中,I2的沸点最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应不需要加热就可以发生 | |
| B. | 反应条件为加热的反应都是吸热反应 | |
| C. | 化学反应放热还是吸热,取决于反应条件 | |
| D. | 化学反应除了生成新物质外,还伴随着能量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物总能量一定低于反应物总能量 | |
| B. | 酒精可用作燃料,说明酒精燃烧是释放能量的反应 | |
| C. | 干冰气化需要吸收大量的热,这个变化是吸热反应 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com