
分析 (1)铜离子变成了亚铜离子,被还原,亚硫酸根被氧化成硫酸根,写成反应,根据化合价升降相等配平方程式;
(2)根据原子守恒及电子转移列出关系式,根据关系式计算样品中FeS2的质量分数;
(3)根据题中信息,铂溶于王水时产生H[AuCl4]和一种无色气体为一氧化氮,据此写出反应的离子方程式.
解答 解:(1)在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热生成了CuCl,亚硫酸根检验还原性,被氧化成硫酸根,根据化合价变化配平方程式可得:2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+,
故答案为:2Cu2++SO32-+2Cl-+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2CuCl↓+SO42-+2H+;
(2)令样品中FeS2的质量分数是x,则:
3FeS2~6SO2~12Fe2+~2Cr2O72-
3×120g 2mol
0.1xg 0.025L×0.02mol/L
所以$\frac{3×120g}{0.1xg}$=$\frac{2mol}{0.025L×0.02mol/L}$,解得,x=90.00%,故答案为:90.00%.
(3)根据题中信息,铂溶于王水时产生[AuCl4]-和一种无色气体为一氧化氮,反应的离子方程式为:Au+NO3-+4H++4Cl-=[AuCl4]-+NO↑+2H2O,故答案为:Au+NO3-+4H++4Cl-=[AuCl4]-+NO↑+2H2O.
点评 考查根据方程式进行的多步计算、方程式的书写等知识,难度较大,注意根据关系式进行计算时清楚反应过程寻找关系式是关键.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
 |  |  |  |  |  |  |
| A. | ②④⑥⑦ | B. | ①④⑤⑥ | C. | ①③⑤⑦ | D. | ①②④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:选择题
将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如图所示。下列叙述正确的是( )

A.在图示的转化中,化合价不变的元素只有铜
B.由图示的转化可得出氧化性的强弱顺序:O2>Fe3+>S
C.在图示的转化中,发生的反应有:H2S+Cu2+=CuS↓+2H+
D.在图示的转化中,发生的反应有:4Fe2++O2+2H2O=4Fe3++4OH-
查看答案和解析>>
科目:高中化学 来源:2017届广西桂林十八中高三上10月月考化学试卷(解析版) 题型:选择题
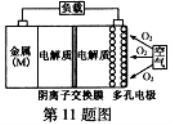
金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH) n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是( )
A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于 氧气扩散至电极表面
氧气扩散至电极表面
 B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C.M–空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D.在M–空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com