

 ,
, ;
;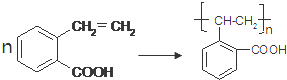 ,
, .
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、1g氢气在氧气中完全燃烧生成气态水,放出热量120.9kJ,氢气的燃烧热大于241.8kJ?mol-1 | |||
B、500℃30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)
| |||
| C、常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |||
| D、已知中和热为-57.3 kJ?mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,PH=9的碳酸钠溶液中由水电离出的c(OH-)=1×10-9mol?L-1 |
| B、温度相同时,在弱酸溶液和强碱稀溶液中,水的离子积常数Kw相同 |
| C、将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| D、中和等体积pH相同的H2SO4和HCl溶液,消耗NaOH的物质的量为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
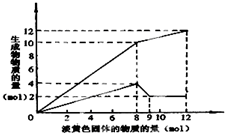 某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种.当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系,如图所示.请填写下列空白:
某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种.当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系,如图所示.请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
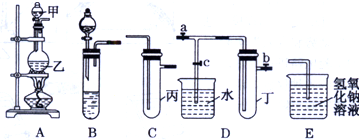
| 实验 序号 | 实验操作 | 现象 |
| Ⅰ | 将氯水滴入品红溶液 | ① |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.7×10-5mol?L-1 |
| HNO2 | 7.1×10-4mol?L-1 |
| HCN | 6.2×10-10mol?L-1 |
| HClO | 4.7×10-8mol?L-1 |
| NH3?H2O | 1.7×10-5mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com