
分析 发生反应为CaCO3+2HCl=CaCl2+H2O+CO2↑,根据n=$\frac{m}{M}$=cV计算出碳酸钙、HCl的物质的量,然后判断过量,根据不足量计算出生成二氧化碳的物质的量、消耗HCl的物质的量及生成氯化钙的物质的量,最后根据V=nVm计算出标准状况下二氧化碳的体积,根据c=$\frac{n}{V}$计算出盐酸、氯化钙的物质的量浓度.
解答 解:10克含杂质10%的石灰石中含有碳酸钙的物质的量为:$\frac{10g×(1-10%)}{100g/mol}$=0.09mol,
100mL 2mol/L的盐酸中含有HCl的物质的量为:2mol/L×0.1L=0.2mol,
根据反应CaCO3+2HCl=CaCl2+H2O+CO2↑可知,0.2molHCl完全反应消耗0.1mol碳酸钙,显然HCl过量,碳酸钙完全反应,
反应生成二氧化碳的物质的量为:n(CO2)=n(CaCO3)=0.09mol,标准状况下0.09mol二氧化碳的体积为:V(CaCO3)=22.4L/mol×0.09mol=2.016L;
反应消耗HCl的物质的量为:0.09mol×2=0.18mol,反应后剩余的HCl为:0.2mol-0.018mol=0.02mol,则反应后溶液中HCl的物质的量浓度为:c(HCl)=$\frac{0.02mol}{0.1L}$=0.2mol/L,
反应后生成氯化钙的物质的量为:n(CaCl2)=n(CaCO3)=0.09mol,反应后溶液中氯化钙的物质的量浓度为:c(CaCl2)=$\frac{0.09mol}{0.1L}$=0.9mol/L,
答:反应生成二氧化碳在标准状况下的体积为2.016L;反应后盐酸的浓度为0.2mol/L,氯化钙溶液的浓度为0.9mol/L.
点评 本题考查了化学方程式的计算,题目难度中等,正确判断过量情况为解答关键,注意掌握物质的量与气体摩尔体积、摩尔质量、物质的量浓度之间的关系,试题培养了学生的化学计算能力.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:解答题
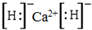 .
.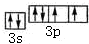 ;D与E能形成一种非极性分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.
;D与E能形成一种非极性分子,该分子的结构式为S=C=S;D所在族元素的氢化物中,沸点最低的是H2S.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠固体溶于水放热 | |
| B. | 红磷在空气中燃烧,产生大量白雾 | |
| C. | 分别蘸有浓盐酸与浓氨水的玻璃棒靠近产生白烟 | |
| D. | 细铁丝在氧气中燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)=c(HA-)+2c(A2-)+c(OH-) | B. | c(H2A)+c(HA-)+c(A2-)=0.2mol•L-1 | ||
| C. | c(H+)•c(OH-)=10-14 | D. | c(A2-)+c(OH-)=c(H+)+c(H2A) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2 NaOH NaHCO3 | B. | NaHCO3 CaCl2 HCl | ||
| C. | AlCl3 MgCl2 NaOH | D. | Ba(OH)2 CaCl2 H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 甲离子 | 乙离子 | 丙试剂 |
| A | SO${\;}_{4}^{2-}$ | CO${\;}_{3}^{2-}$ | 稀盐酸、Ba(NO3)2的混合溶液 |
| B | Cl- | CO${\;}_{3}^{2-}$ | AgNO3溶液、稀硝酸 |
| C | H+ | Na+ | 酚酞试液 |
| D | Mg2+ | Na+ | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 装置 |  |  | 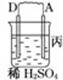 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com