
同一周期X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性是: HXO4 >H2YO4 >H3ZO4,则下列判断错误的是
| A.原子半径:X > Y > Z | B.气态氢化物的稳定性:HX > H2Y > ZH3 |
| C.非金属性:X > Y > Z | D.阴离子的还原性:Z3- > Y2- > X- |
科目:高中化学 来源: 题型:单选题
N、O、Si、S是重要的非金属元素,下列说法正确的是
| A.N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱 |
| B.氮的氧化物和硫的氧化物既是形成光化学烟雾,又是形成酸雨的主要物质 |
| C.S、SO2和Si、SiO2四种物质均能与NaOH溶液反应,各自又能与某些酸反应 |
| D.N、Si、S的单质均能和氧气反应,生成的产物分别是NO2、SiO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
原子结构模型的演变图中,①为道尔顿实心球式原子模型、②为卢瑟福带核的原子模型、③为汤姆生葡萄干面包式原子模型、④为玻尔轨道式原子模型。其中符合历史演变顺序的一组排列是( )
① ② ③ ④
| A.①③②④ | B.①②③④ |
| C.①④③② | D.①③④② |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )
| | | X |
| | Y | |
| Z | | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素的离子aW2+、bX+、cY2-、dZ-具有相同的电子层结构,下列推断正确的是
| A.热稳定性:H2Y<HZ | B.原子半径:W>X>Z>Y |
| C.离子半径:W2+>Y2- | D.碱性:XOH<W(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各选项中两种粒子所含电子数不相等的是
| A.羟甲基(-CH2OH)和甲氧基(CH3O-) |
| B.羟基(-OH)和氢氧根(OH-) |
| C.硝基(-NO2)和二氧化氮(NO2) |
| D.亚硝酸(HNO2)和亚硝酸根(NO2—) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分,每空1分)下表是元素周期表的一部分,回答下列有关问题: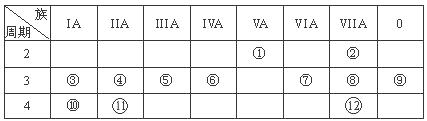
(1)写出下列元素符号:① ,⑥ ,⑦ 。
(2)画出原子的结构示意图:④ ,⑧ 。
(3)在①~?元素中,金属性最强的元素是 ,非金属性最强的元素是 ,最不活泼的元素是 。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同 b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是 (用元素符号表示),跟它同周期的ⅦA元素是 (用元素符号表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com