
| A. | 反应物的浓度 | B. | 反应是否为可逆反应 | ||
| C. | 反应是否使用催化剂 | D. | 反应物的性质 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于24s | B. | 等于20s | C. | 大于20s | D. | 小于20s |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )
如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )| A. | 向A池中通入4.48 L HCl气体可恢复到电解前的状态 | |
| B. | 停止通电后恢复至室温A池中溶液的pH值为14 | |
| C. | 电极e应为粗铜板材料且质量减少6.4 g | |
| D. | 该电路中通过的电子的物质的量为0.4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
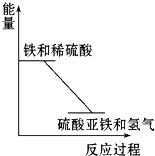 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +2Ag[(NH3)2]OH
+2Ag[(NH3)2]OH
 +2Ag+3NH3+H2O
+2Ag+3NH3+H2O ,通过类似反应柠檬烯可由一种有机物合成得到,该有机物的结构简式为
,通过类似反应柠檬烯可由一种有机物合成得到,该有机物的结构简式为 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com