
| A、1mol/L氯化铜溶液中的Cu2+数小于NA |
| B、标准状况下,22.4L Cl2参加任何化学反应转移的电子数都是2NA |
| C、28 g聚乙烯含有的碳原子数为2NA |
| D、1mol CH5+所含电子数为8NA |


科目:高中化学 来源: 题型:
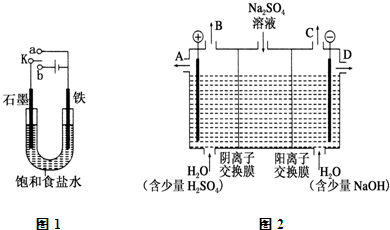 (1)某课外活动小组同学用如图1装置进行实验,试回答下列问题:
(1)某课外活动小组同学用如图1装置进行实验,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba(NO3)2溶液中通入过量的SO2:3SO2+3Ba2++2NO3-+2H2O=3BaSO4+4H++2NO↑ |
| B、酸性高锰酸钾溶液中滴加H2O2溶液:4MnO4-+4H2O2+12H+=4Mn2++7O2+10H2O |
| C、溴化亚铁溶液中通入少量的氯气::2Fe2++4Br-+3Cl2=3Fe3++2Br2+6Cl- |
| D、Fe2(SO4)3溶液中加入足量的Na2S溶液:2Fe3++3S2-=2FeS↓+S↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液中:2c(R2-)+c(HR-)=c(Na+) |
| B、若0.3 mol/L HY溶液与0.3 mol/L NaOH溶液等体积混合后,溶液的pH=9,则:c(OH-)-c(HY)=c(H+)=1×10-9mol/L |
| C、0.2mol?L-1 HCl溶液与等体积0.05 mol?L-1 Ba(OH)2溶液混合后,溶液的pH=1 |
| D、NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | W | Y | Z | Q |
| 原子半径(×10-12m) | 37 | 64 | 66 | 70 | 154 |
| 主要化合价 | +1 | -1 | -2 | +5、-3 | +1 |
| A、由Q与Y形成的化合物中只存在离子键 |
| B、Z与X之间形成的化合物具有还原性 |
| C、由X、Y、Z三种元素形成的化合物,其晶体一定是分子晶体 |
| D、Y与W形成的化合物中,Y显负价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
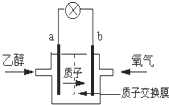 美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200°C左右供电.电池总反应为:C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是( )
美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200°C左右供电.电池总反应为:C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是( )| A、a极为电池的正极 |
| B、电池工作时电流由b极沿导线经灯泡再到a极 |
| C、电池正极的电极反应为:4H++O2+4e-=2H2O |
| D、电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L HF中含有的氟原子数目为NA(NA表示阿伏加德罗常数) |
| B、0.1mol/L的NH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+) |
C、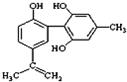 1mol如图所示物质与浓溴水反应时通常最多消耗Br2为4mol |
| D、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0,一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝片与NaOH溶液反应:2OH-+Al═AlO2-+H2↑ |
| B、向AgCl悬浊液中滴加NaI溶液,白色沉淀变成黄色:AgCl+I-═AgI+Cl- |
| C、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
| D、将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 过渡态理论认为:化学反应并不是通过简单的碰撞就能完成的,而是从反应物到生成物的过程中经过一个高能量的过渡态.如图1是1mol NO2与1mol CO恰好反应生成CO2和NO过程中的能量变化示意图.
过渡态理论认为:化学反应并不是通过简单的碰撞就能完成的,而是从反应物到生成物的过程中经过一个高能量的过渡态.如图1是1mol NO2与1mol CO恰好反应生成CO2和NO过程中的能量变化示意图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com