
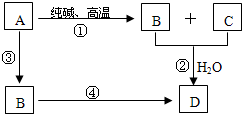
 已知A是一种不溶于水的固体非金属氧化物,根据下列转化关系回答下列各题:
已知A是一种不溶于水的固体非金属氧化物,根据下列转化关系回答下列各题:

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度/(mol?L-1) | 1 | 1 | 2 | 1 |
| A、Na+ |
| B、Ba2+ |
| C、F- |
| D、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 咖啡酸(如图)存在于野胡萝卜、光叶水苏、荞麦等物中.咖啡酸有止血作用,特别对内脏的止血效果较好.
咖啡酸(如图)存在于野胡萝卜、光叶水苏、荞麦等物中.咖啡酸有止血作用,特别对内脏的止血效果较好.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 氢氧燃料电池的实验装置如图所示,回答下列有关该实验的问题.
氢氧燃料电池的实验装置如图所示,回答下列有关该实验的问题.查看答案和解析>>
科目:高中化学 来源: 题型:
 ,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.写出B4转化为B2的热化学方程式:
,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.写出B4转化为B2的热化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| m |
| n |
| m |
| n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com