
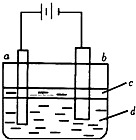
 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.

科目:高中化学 来源: 题型:
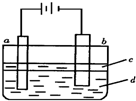 由于Fe(OH)2极易被氧化,实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用下图实验装置可制得纯净的Fe(OH)2沉淀,两极材料分别为石墨和铁.下列有关叙述正确的是( )
由于Fe(OH)2极易被氧化,实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用下图实验装置可制得纯净的Fe(OH)2沉淀,两极材料分别为石墨和铁.下列有关叙述正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
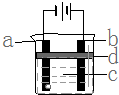 由于Fe (OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe (OH)2沉淀,应用如图电解实验可以制得白色的纯净的Fe (OH)2沉淀.两电极材料分别为石墨和铁.
由于Fe (OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe (OH)2沉淀,应用如图电解实验可以制得白色的纯净的Fe (OH)2沉淀.两电极材料分别为石墨和铁.查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ.用标准NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作中会导致实验结果偏低的是
Ⅰ.用标准NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作中会导致实验结果偏低的是查看答案和解析>>
科目:高中化学 来源:2011-2012学年内蒙古巴彦淖尔市中学巴市一中高二上学期12月月考化学试卷 题型:填空题
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液跟烧碱反应制得白色纯净的Fe(OH)2沉淀,应用如图所示装置可以制得白色纯净的Fe(OH)2沉淀。两极材料分别为铁和石墨。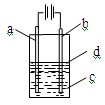
(1)a电极材料应为 ,电极反应式为 。
(2)电解液c最好是 (填编号)。
| A.纯水 | B.AgNO3溶液 | C.NaOH溶液 | D.CuCl2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com