
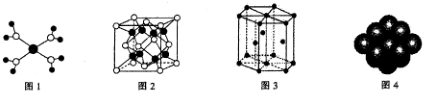
| A. | 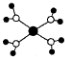 水合铜离子的模型如图所示,1个水合铜离子中含有4个配位键 | |
| B. | 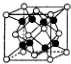 K2O晶体的晶胞如图所示,每个K2O晶胞平均占有8个O2- | |
| C. | 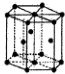 金属Zn中Zn原子堆积模型如图所示,空间利用率为68% | |
| D. |  金属Cu中Cu原子堆积模型如图,为面心立方最密堆积,每个Cu原子的配位数均为8 |
分析 A.水合铜离子中铜离子的配位数为4,配体是水,水中的氧原子提供孤电子对与铜离子形成配位键;
B.根据均摊法可知,在K2O晶体的晶胞中,每个K2O晶胞平均占有8×$\frac{1}{8}$+6×$\frac{1}{2}$=4个O2-;
C.金属Zn中Zn原子堆积模型为立方最密堆积方式;
D.根据晶胞图可知,铜原子分布在晶胞的顶点和面心上.
解答 解:A、水合铜离子中铜离子的配位数为4,配体是水,水中的氧原子提供孤电子对与铜离子形成配位键,1个水合铜离子中有4个配位键,故A正确;
B、根据均摊法可知,在K2O晶体的晶胞中,每个K2O晶胞平均占有8×$\frac{1}{8}$+6×$\frac{1}{2}$=4个O2-,故B错误;
C、金属Zn中Zn原子堆积模型为立方最密堆积方式,空间利用率为74%,故C错误;
D、在金属晶体的最密堆积中,对于每个原子来说,在其周围的原子有与之同一层有六个原子和上一层的三个及下一层的三个,故每个原子周围都有12个原子与之相连,对于铜原子也是如此,所以每个Cu原子的配位数均为12,故D错误;
故选A.
点评 本题考查了配合物、离子晶体、最密堆积等知识,难度不大,解题关键是对图要仔细观察,同时正确理解基本概念.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:选择题
| A. | SiO2是还原剂 | |
| B. | 氧化剂与还原剂的物质的量比为2:1 | |
| C. | 此反应中电子转移4mol | |
| D. | CO是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
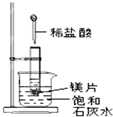 如图所示,把试管放入盛有 25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入 5mL 盐酸于试管中,试回答下列问题:
如图所示,把试管放入盛有 25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入 5mL 盐酸于试管中,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有氧化性,可用于漂白纸浆 | B. | NH4HCO3含有氮元素,可用作氮肥 | ||
| C. | Fe2(SO4)3易溶于水,可用作净水剂 | D. | Al2O3硬度大,可用作耐高温材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:4 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定不含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同时含有分子和离子的电解质溶液,一定是弱电解质溶液 | |
| B. | pH=3的盐酸中,其c(H+)是pH=1的盐酸中的3倍 | |
| C. | 0.1 mol/L KOH溶液和0.1 mol/L 氨水中,其c(OH-)相等 | |
| D. | 室温时,pH=3的硫酸和pH=11的氨水等体积混合,混合溶液的pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
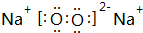 (用电子式表示)
(用电子式表示)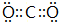 (用电子式表示)
(用电子式表示)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com