
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ����ø�Ũ��������480 mL�� 1 mol/L��ϡ���ᡣ�ɹ�ѡ�õ������У�����ƿ���ձ��۲�������ҩ�ע���Ͳ

��ش��������⣺
��1����Ũ��������ʵ���Ũ��Ϊ____________ mol/L��
��2������ϡ����ʱ�����������в���Ҫ��������____________������ţ�����ȱ�ٵ�������______________________________ (��д��������)��
��3�������㣬����480mL��1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ______ mL����ȡŨ�������õ���Ͳ�Ĺ����________��
(�����й����ѡ�ã� 10 mL���� 25 mL���� 50 mL����100 mL)
��4���������Ƶ�ϡ������вⶨ��������Ũ�ȴ���1mol/L�����ƹ��������и�������������������ԭ����____________��
A������ʱ����������ƿ�̶��߽��ж���
B�����ձ��н�Ũ�������ϡ�ͺ�����ת������ƿ��
C��ת����Һʱ��������������Һ��������ƿ����
D������ƿ������ˮϴ�Ӻ�δ���������������ˮ
E������ҡ�Ⱥ���Һ����ڿ̶��ߣ��ټ�����ˮ���̶���
���𰸡� 18.4 �٢� ��ͷ�ιܡ�500mL ����ƿ 27.2 50 mL A B
��������(1)��Һ�����ʵ���Ũ��Ϊ��c=![]() =
=![]() =18.4mol/L���ʴ�Ϊ��18.4��
=18.4mol/L���ʴ�Ϊ��18.4��
(2)���������м��㡢��ȡ��ϡ�͡�ϴ�ӡ����ݡ�ҡ�ȵȲ�����һ������Ͳ��ȡŨ���ᣬ���ձ���ϡ��(������Ͳ��ȡˮ�����ձ�)�����ò��������裬��ȴ��ת�Ƶ�500mL����ƿ(������480mL����ƿ����ѡ��500mL����ƿ)�У����ò�����������ϴ���ձ���������2-3�Σ�����ϴ��Һ��������ƿ�У���ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�����ݵߵ�ҡ�ȣ�����������������Ͳ���ձ�����������500mL����ƿ����ͷ�ιܣ��ò���������ƿ��ҩ�ף���ȱ�ٵ�����Ϊ��ͷ�ιܡ�500mL����ƿ���ʴ�Ϊ���٢�����ͷ�ιܡ�500mL����ƿ��
(3)������480mL����ƿ����ѡ��500mL����ƿ������480mL 1molL-1��ϡ���ᣬ����Ҫ��Ũ��������ΪVmL��������Һϡ�Ͷ���CŨVŨ=CϡVϡ��֪��18.4mol/L��VmL=1molL-1��500mL�����V=27.2mL��Ӧ��ѡ��50mL����Ͳ��ȡ���ʴ�Ϊ��27.2��50 mL��
(4)A������ʱ����������ƿ�̶��߽��ж��ݣ��ʵ���ϡ��Һ���ƫС������c=![]() �жϿ�֪Ũ��ƫ�ߣ���A��ȷ��B����ϡ�ͺ��ϡ��������ת������ƿ�����žͽ����Ժ��ʵ�������һ����ȴ����������ϡ��Һ���ƫС������c=
�жϿ�֪Ũ��ƫ�ߣ���A��ȷ��B����ϡ�ͺ��ϡ��������ת������ƿ�����žͽ����Ժ��ʵ�������һ����ȴ����������ϡ��Һ���ƫС������c=![]() �жϿ�֪Ũ��ƫ�ߣ���B��ȷ��C��ת����Һʱ��������������Һ��������ƿ���棬����Ũ��Һ���ʵ���ƫС������c=
�жϿ�֪Ũ��ƫ�ߣ���B��ȷ��C��ת����Һʱ��������������Һ��������ƿ���棬����Ũ��Һ���ʵ���ƫС������c=![]() �жϿ�֪Ũ��ƫ�ͣ���C����D������ƿ������ˮϴ�Ӻ�δ���������������ˮ�����ƹ�������Ҫ�μ�����ˮ���ʴ���Ӱ�죬��D����E�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ��㲹�伸��ˮ���̶ȴ�������ϡ��Һ���ƫ����c=
�жϿ�֪Ũ��ƫ�ͣ���C����D������ƿ������ˮϴ�Ӻ�δ���������������ˮ�����ƹ�������Ҫ�μ�����ˮ���ʴ���Ӱ�죬��D����E�����ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ��㲹�伸��ˮ���̶ȴ�������ϡ��Һ���ƫ����c=![]() �жϿ�֪Ũ��ƫ�ͣ���E����ѡAB��
�жϿ�֪Ũ��ƫ�ͣ���E����ѡAB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһ�����ʵ���Ũ�ȵ�NaOH��Һ100mL��Ȼ������ͨ��һ������CO2���壬�õ���ҺA����A����λ�������0.1 molL-1��HCl��Һ��������CO2�����������״����������HCl��Һ�����֮���ϵ��ͼ��ʾ��ͨ������ش�
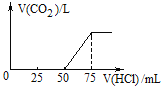
��1��A��Һ�е�����Ϊ_________����ѧʽ���������ʵ���֮����_______��
��2��ͨ��CO2�������__________________����״������
��3��NaOH��Һ�����ʵ���Ũ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������岻��ȱ�ٵ���Ԫ�أ����뺬���Ļ�����ɲ��������������ơ����г���һ�ֳ����IJ���ҩ���ͼ1������˵���飺 
��ҩƷ��Fe2+�Ỻ�����������ҹ涨��ҩ����Fe2+�������ʳ���10%�������ٷ��ã�
��1��Ϊ�˼���ijҩ����۵ġ������ơ��Ƿ�������ʵ���ҿ�ѡ�õ�������������ļ����Լ�Ϊ�����Լ������ƣ���
��2��ʵ���Ҳ���H2SO4�ữ��KMnO4��Һ�ԡ������ơ��е�Fe2+���еζ�������ҩƷ�������ɷֲ���KMnO4��Ӧ�����÷�Ӧ�����ӷ���ʽΪ�� ��
��3��������������Ԫ����������Ϊ20.00%�ġ������ơ�19.00g������ȫ������ϡ�����У����Ƴ�1000.00mL��Һ��ȡ��20.00mL����0.01300mol/L��KMnO4��Һ�ζ�������KMnO4��Һ�����ͼ2��ʾ��
��ʵ��ǰ������Ҫ��ȷ����0.01300mol/L KMnO4��Һ250mL������ʱ��Ҫ�IJ������������������ձ�����ͷ�ι��⣬���� ��
��ijͬѧ�ĵζ���ʽ���гֲ�����ȥ����ͼ����������� �� 
����ͼ��֪����KMnO4��Һ���ΪmL��
�ܵζ��յ�۲쵽������Ϊ��
���Ա�KMnO4��Һ�ζ���Ʒ��Һ��Ũ�ȣ��ж����²���������ʵ����ƫС���� ��
A���ζ������У���ƿ��̫���ң�������Һ�ν���
B��δ�ñ�KMnO4��Һ��ϴ�ζ���
C���ζ��ӽ��յ�ʱ������������ˮ��ϴ��ƿ�ڱ�
D���ζ�ǰ���ӣ��ζ����ӣ���Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����в�ҩ�ķ�Դ�أ�Ŀǰ�й���Լ��12000��ҩ��ֲ���ij�в�ҩ��ȡ���л���ṹ��ͼ��ʾ�����л��������˵���в���ȷ���ǣ� �� 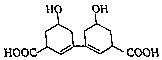
A.����ʽΪC14H18O6
B.������ԭ�ӵ�һ��ȡ����5��
C.1mol���л����������Ľ����Ʒ�Ӧ����4mol H2
D.���Ӽ��ܷ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֱ���ŷź�SO2���������γ����꣬Σ��������ij��ѧʵ��С����������й�SO2���ʵ�̽����� 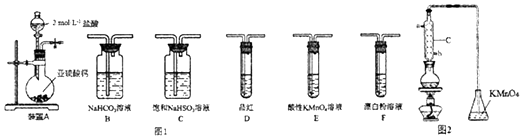
��1��װ��A�з�Ӧ�����ӷ���ʽΪ ��
��2��ѡ��ͼ1����װ�ú�ҩƷ̽��������������������ǿ����
�ټ�ͬѧ��Ϊ����A��C��F��β������˳������װ�ÿ���֤��������ʹη��������ǿ������ͬѧ��Ϊ�÷������������������� ��
�ڱ�ͬѧ��Ƶĺ���ʵ������Ϊ������A��C��β������������ĸ��˳������װ�ã�����װ��C�������� �� ֤�������������ǿ�ڴ���������Ե�ʵ�������� ��
��3��������ͼ2 ��װ��A���Һ��SO2�ĺ�������ȡ10.00mL��Һ��Բ����ƿ�У�����ʹSO2ȫ����������20.00mL 0.1000mol/L��KMnO4����Һ���գ���ַ�Ӧ������0.200Omol/L��KI��Һ�ζ�������KMnO4 �� ����KI��Һ25.00mL��
����֪��5SO2+2MnO4��+2H2O=2Mn2++5SO42��+4H+ �� 10I��+2MnO4��+16H+=2Mn2++5I2+8H2O��
�ٸ�װ��������C������Ϊ �� ˮͨ��C�Ľ���Ϊ ��
�ڲ�Һ��SO2�ĺ���Ϊmol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¡�0.2mol/L��һԪ��HA���Ũ�ȵ�NaOH��Һ�������Ϻ�����Һ���Ϊ����֮�ͣ���������Һ�в�������ּ�Ũ����ͼ��ʾ������˵������ȷ���ǣ� �� 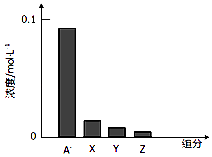
A.HA������
B.�û��ҺpH��7
C.�û����Һ�У�c��A����+c��Y��=c��Na+��
D.ͼ��X��ʾHA��Y��ʾOH�� �� Z��ʾH+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ζ�ʵ���йص�˵������ȷ���ǣ� ��
A.����ƿ�͵ζ��ܶ���Ҫ���Լ���ϴ
B.��NaOH�ζ�����ʱ�����ζ�����ʱ���ӿ̶ȣ��ᵼ�²ⶨ���ƫ��
C.�õζ���ȷ��ȡ20.0 mL����
D.��KMnO4�ζ�����������Һ��ʵ���в���Ҫ�������ָʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϲ�����������ȥ��������(��Ҫ�ɷ�ΪFe2O3��FeO��SiO2��Al2O3����������������)��ȡ��ˮ����������(FeSO4��7H2O)���������£�

(1)����I����Ҫ�ɷ���_______________(�ѧʽ)��
(2)��ԭʱ���Լ�X��ѡ��SO2����Ӧ����Һ�е���������_________________(�ѧʽ)
(3)������ˢ�õ�����Һ�д���Fe3+�ķ�����____________________��
(4)��ˮ����������(FeSO4��7H2O)��ҽѧ�ϳ�������Ѫ����ij����С��ͨ������ʵ�鷽���ⶨij��Ѫ�����������ӵĺ�����
����a��ȡ10Ƭ��Ѫ����Ʒ��ȥ���¡���ĥ���ܽ⡢���ˣ�����Һ���250mL��Һ��
����b��ȡ������Һ25 mL����ƿ�У���������ϡ�����ữ���μ�0.0100 mol/L��KMnO4��Һ����ǡ����ȫ��Ӧ����¼���ĵ�KMnO4��Һ��������ٶ�ҩƷ�������ɷֲ���KmnO4��Ӧ)�������ķ�ӦΪ��MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O��
����c���ظ�������b��2��3�Σ�ƽ������KMnO4��Һ20.00mL��
������a��������Һʱ��Ҫ�IJ����������ձ�����ͷ�ι��⣬����Ҫ___________��________��
�ڸò�Ѫ�����������ӵĺ���Ϊmg/Ƭ����д���������) ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ����ȡClO2 �� ����ClO2Ϊԭ���Ʊ��������ƣ�NaClO2��һ�ָ�Ч��������Ư��������֪��NaClO2������Һ���¶ȵ���38��ʱ�����ľ�����NaClO23H2O������38��ʱ����������NaClO2 �� ����60��ʱNaClO2�ֽ��NaClO3��NaCl�� 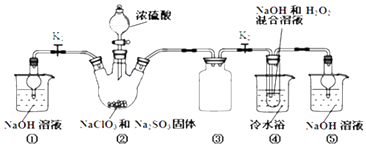
���������գ�
��1��װ�â��в���ClO2�Ļ�ѧ����ʽΪ��װ�â��з�����Ӧ�����ӷ���ʽΪ ��
��2��װ�â۵���������װ�âٺ͢��ڱ�ʵ���е����� ��
��3��װ�âܷ�Ӧ�����Һ�л���������NaOH���ʣ��Ӹ���Һ�����ˮNaClO2����IJ�������Ϊ���ټ�ѹ��55�����������ᾧ���ڳ��ȹ��ˣ�����50�����ҵ���ˮϴ�ӣ��ܵ���60�����õ���Ʒ�����������50�����ҵ���ˮϴ�ӵ�ԭ���� ��
��4���������ƴ��Ȳⶨ����ȷ��ȡ��������������Ʒ10.0g���ձ��У�������������ˮ�����ĵ⻯�ؾ��壬�ٵ���������ϡ���ᣬ��ַ�Ӧ�������û��Һ���250mL������Һ����ȡ25.00mL����Һ����2.0 molL��1Na2S2O3��Һ�ζ���I2+2S2O32��=2I��+S4O62�������Ե�����Һ��ָʾ�����ﵽ�ζ��յ�ʱ������Ϊ �� �ظ��ζ�3�Σ�������������ʾ�������Ʒ��NaClO2����������Ϊ ��
ʵ����� | �ζ�ǰ����/mL | �ζ������/mL |
1 | 0.00 | 19.96 |
2 | 3.26 | 23.30 |
3 | 1.10 | 23.40 |
��5��ʵ���������NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ������NaClO2 �� ����һ�ݼ��ȸ���60��ʹ֮���ʣ���һ���ϸ棬�������Һ�����ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ��������ͬ��������ͬ�������жϡ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com