
����Ŀ��ij��ȤС���������ͼ��ʾ��ʵ��װ�ã��ȿ�������ȡ���壬�ֿ�������֤���ʵ����ʡ�
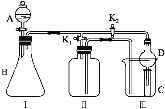
��1����K1�ر�K2������ȡijЩ���塣��ͬѧ��Ϊװ�â��������ȡH2��NH3��O2����װ�â�ֻ���ռ�H2��NH3�������ռ�O2����������_____����ͬѧ��Ϊ�ڲ��Ķ�װ�â�������ǰ���£���װ�â�����ʵ��Ľ���Ҳ���ռ�O2������Ϊ���ĸĽ�������_____��
��2����K2�ر�K1���ܱȽ�һЩ���ʵ����ʡ���ͬѧ���ʵ��Ƚ������ԣ�KClO3��Cl2��Br2����A�м�Ũ�����һ��ʱ�䣬�۲쵽C�е�������______������D�ڸ�װ���е�������_______����Bװ���з�����Ӧ�����ӷ���ʽΪ______����ͬѧ��ʯ��ʯ�����ᡢ�����Ƶ�ҩƷ�������һʵ�顣����ʵ��Ŀ����_____��
��3��ʵ���ҳ���ŨH2SO4�������Ʒ�Ӧ��ȡHNO3������װ�������ʺ���ȡHNO3����_____��ʵ����������Ũ����ķ�����_______��
a 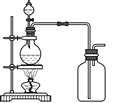 b
b 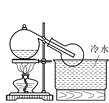 c
c 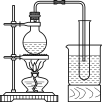 d
d 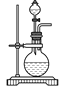
���𰸡��������ܶȱȿ����� ��װ�â���װ��ˮ ��Һ�ʳ�ɫ ��ֹ���� ClO3��+6H++5Cl��=3Cl2��+3H2O �Ƚϴ��ᡢ̼��ͱ��ӵ�����ǿ����ʵ֤���ԣ�CH3COOH��H2CO3��C6H5OH�� b ʢװ�ڴ�����������ɫϸ�ڲ���ƿ�У����������������������µĵط���
��������
��1�������ܶȱȿ��������ſ������ռ������������ſ������ռ�����װ���н����̣ܶ������ܳ���Ϊ�����ſ�����������ˮ�������ռ�O2�����壻
��2��װ�â���֤���ʵ�����(K2��K1�ر�)������������+��ԭ��=��������+��ԭ��������ԣ�������>���������ԭ�ԣ���ԭ��>��ԭ�����Ҫ���ʵ��֤��������KClO3>Cl2>Br2����I�з���KClO3��Ũ�����������ԭ��Ӧ�����з���������NaBr��������ԭ��Ӧ���л������õ�װ���ܷ�ֹ��������Bװ����KClO3��-1�۵������������������·���������ԭ��Ӧ��������������ǿ�������ᣬʯ��ʯ�ʹ��ᷴӦ���ɶ�����̼��������̼�ͱ����Ʒ�Ӧ���ɱ��ӣ��ݴ˷���ʵ��Ŀ�ģ�
(3)�ٸ��ݻ�ѧ��Ӧԭ�����������ȡԭ���ǣ������Һ������ȡ���ѻӷ��Ե�������ȡ�ӷ��Ե��ᣬ�ݴ�ѡ��װ�ã�
�ڸ������������ѡ����ʵ����淽�����������ֽ⣬����ʱ���ܼ��⣬�����¼��ɷֽ⣬��Ҫ���±��档
��1����ͬѧ����װ���н����̣ܶ������ܳ���Ϊ�����ſ�������O2���ܶȴ��ڿ������ܶȣ�������Ӧ���������ſ������ռ�����ͬѧ��O2������ˮ������Ӧ������������ˮ�������ܲ�����ˮ���ռ������ԸĽ������ǽ�װ�â���װ��ˮ��
�ʴ�Ϊ���������ܶȱȿ�����װ�â���װ��ˮ��
��2������������+��ԭ��=��������+��ԭ��������ԣ�������>���������ԭ�ԣ���ԭ��>��ԭ�����Ҫ���ʵ��֤��������KClO3>Cl2>Br2��װ�â���֤���ʵ�����(K2��K1�ر�)����I�з���KClO3��Ũ�����������ԭ��Ӧ�����з���������NaBr��������ԭ��Ӧ����������Ϊ������>���������A��ΪŨ���ᣬB��ΪKClO3���壬C��ΪNaBr��Һ���۲쵽C�е�����Ϊ��Һ�ʳ�ɫ������DΪ����ܣ��л������ã������ܷ�ֹ��������Bװ������������Ӻ������������������·�����̬���з�Ӧ������������ӦΪ��ClO3��+6H++5Cl��=3Cl2��+3H2O��ʯ��ʯ�ʹ��ᷴӦ���ɶ�����̼��������̼�ͱ����Ʒ�Ӧ���ɹ������������B�й����ܽ⣬������ɫ���壬C�Թ��в�����ɫ������ʵ���Ŀ���DZȽ�̼�ᡢ���ᡢ���ӵ�����ǿ��(ʵ֤���ԣ�CH3COOH��H2CO3��C6H5OH)��
�ʴ�Ϊ����Һ�ʳ�ɫ����ֹ������ ClO3��+6H++5Cl��=3Cl2��+3H2O���Ƚϴ��ᡢ̼��ͱ��ӵ�����ǿ��(ʵ֤���ԣ�CH3COOH��H2CO3��C6H5OH)��
(3)���������ȡԭ���ǣ������Һ������ȡ����d���÷�Ӧ�����ѻӷ��Ե�������ȡ�ӷ��Ե��ᣬ�����ӷ����������ſ������ռ�����a��c������������Ļӷ���ע����ѡ����ռ�������bװ����ʾ��
�ʴ�Ϊ��b��
�ڴ����������Ũ�����ڳ����¼�������Ⱦͻ�ֽ����ɶ���������������ˮ������ʱ��Ҫ������ʹ����ɫ���Լ�ƿ��
�ʴ�Ϊ��ʢװ�ڴ�����������ɫϸ�ڲ���ƿ�У�������������(�������µĵط�)��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ý���ʵ�飬����˵����ȷ����
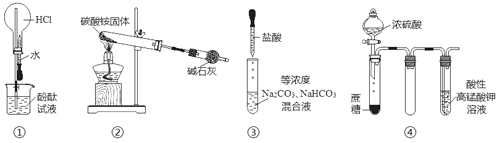
A. ʵ��ٿɹ۲쵽��ɫ��Ȫ
B. ʵ��ڿ��ռ�����������
C. ʵ�������εμ�ϡ����ʱ���Թ�������������������
D. ʵ���������KMnO4��Һ���д������ݳ��֣�����Һ��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����ö��������Ʊ��輰�仯��������̣�����˵����ȷ���ǣ�������
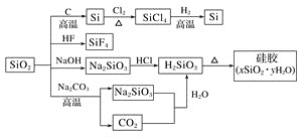
A.SiO2��������������
B.ʢ��NaOH��Һ���Լ�ƿ���ò�����
C.�轺��ˮ����ظ�����
D.ͼ����ʾת����Ӧ����������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ�������
A. CS2 Ϊ�ռ乹��ΪV�εļ��Է���
B. ˫ԭ�ӻ��ԭ���γɵ����嵥���У�һ��������������������
C. ��ԭ�ӵ����Ƶ�һ��С�ڵ��ʾһ������
D. HCN��SiF4��SO32�� ������ԭ�Ӿ�Ϊsp3�ӻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����ڹ�ũҵ�����о��й㷺Ӧ�ã���ش��������⣺
��1����̬��ԭ�ӵĺ�������Ų�ʽΪ_____________��
��2��Cr3�����γ�������[Cr(H2O)��H2NCH2CH2NH2��]3����������H2NCH2CH2NH2 �в��� sp3�ӻ���ԭ����_____��
��3���Ȼ�������CrO2Cl2���۵㣺-96.5�棬�е㣺117�棬���� CS2 �Ȼ��ܣ����̬ CrO2Cl2����________���塣��֪ NO2���� CS2 ��Ϊ�ȵ����壬�� 1molNO2���к���������ĿΪ ____________
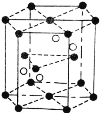
��4��Cr2O3 �����ṹ��ͼ��ʾ����֪ Cr2O3 ��Ħ������Ϊ M g/mol,������ܶ�Ϊ�� g��cm��3 ���������Ϊ V cm3. �����ṹʾ��ͼ�е�С�������_____�����������������������������������ӵ�����NA=_________mol-1(�ú� M, V, ���Ĵ���ʽ��ʾ ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 25 mL 1.00 mol/L HCl ��Һ����μ���δ֪Ũ�� NaOH ��Һ V mL������Һ������Ⱥ��ڱ��¸��ȵ������²�������¼�����Һ���¶ȣ�ʵ������ͼ��ʾ������������ȷ����
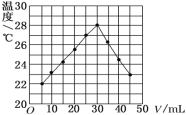
A.����ʵ��ʱ�����¶�Ϊ22��
B.����30 mLNaOH ��Һʱ��HCl��ȫ���к�
C.NaOH ��Һ�����ʵ���Ũ��ԼΪ1.0 mol/L
D.��ʵ��������ܿ���ת��Ϊ��ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ķ���ʽΪC8H10����������ˮ�в���ʹ��ˮ��ɫ�������������Ը��������Һȴ��ʹ����ɫ�����л��ﱽ���ϵ�һ�ȴ���ֻ��1�֣��������(�� ��)
A. 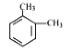 B.
B. ![]() C.
C. 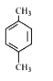 D.
D. 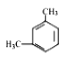
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͽ���һ����̼�ϳɿ�������Դ�״���
(1)��֪����.3CO(g)��6H2(g)![]() CH3CH��CH2(g)��3H2O(g) ��H1����301.3kJ/mol��
CH3CH��CH2(g)��3H2O(g) ��H1����301.3kJ/mol��
��.3CH3OH(g)![]() CH3CH��CH2(g)��3H2O(g) ��H2����31.0kJ/mol��
CH3CH��CH2(g)��3H2O(g) ��H2����31.0kJ/mol��
��CO��H2�ϳ���̬�״����Ȼ�ѧ����ʽΪ___________________________________
(2)ij����С����Cu2O/ZnO�������������£���500��ʱ���о���n(H2)��n(CO)�ֱ�Ϊ2��1��5��2ʱCO��ת���ʱ仯���(��ͼ1��ʾ)����ͼ�б�ʾn(H2)��n(CO)��2��1�ı仯����Ϊ___________(�����a��������b��)��ԭ����_______________________________��
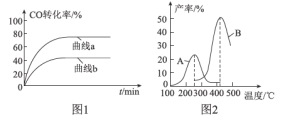
(3)ij����С�����ܱ������г���һ������CO��H2�ϳ���̬�״����ֱ���A��B���ֲ�ͬ���������·�����Ӧ��һ��ʱ�����CH3OH�IJ������¶ȵĹ�ϵ��ͼ2��ʾ������˵����ȷ����____________(��ѡ����ĸ)��
a.ʹ�ô���A�ܼӿ���ػ�ѧ��Ӧ���ʣ�������A��δ���뷴Ӧ
b.�ں��º�ѹ��ƽ����ϵ�г��������CH3OH�IJ��ʽ���
c.��2v(CO)����v(H2)��ʱ����Ӧ�ﵽƽ��״̬
(4)һ���¶��£����ݻ���Ϊ2L�����������ܱ������У������·�ʽ���뷴Ӧ�һ��ʱ���ﵽƽ�⡣

��������ƽ��������ѹǿΪ��ʼʱ��![]() ������¶��£��÷�Ӧ��ƽ�ⳣ��K��______��Ҫʹƽ��������������������ͬ��ֵ����������ȣ�����ʼʱά�ֻ�ѧ��Ӧ���淴Ӧ������У�����������c��ȡֵ��ΧΪ_____________________________________��
������¶��£��÷�Ӧ��ƽ�ⳣ��K��______��Ҫʹƽ��������������������ͬ��ֵ����������ȣ�����ʼʱά�ֻ�ѧ��Ӧ���淴Ӧ������У�����������c��ȡֵ��ΧΪ_____________________________________��
(5)CO���ճ�����������ء�
�ټ������β����CO����������CO�����ǣ�����ԭ��������ȼ�ϵ�أ����е������������(Y2O3)�������(ZrO2)���壬�ܴ���O2�������ĵ缫��ӦʽΪ__________________��
��̼����״�[(CH3O)2CO]����С����һ����ɫ������Ʒ����CO�ϳ�(CH3O)2CO����绯ѧ�ϳ�ԭ��Ϊ4CH3OH��2CO��O2![]() 2(CH3O)2CO��2H2O��װ����ͼ3��ʾ��
2(CH3O)2CO��2H2O��װ����ͼ3��ʾ��
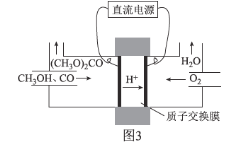
д�������ĵ缫��Ӧʽ��________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�������Դ������CO��ˮ������Ӧ�Ʊ����������仯����ͼ��ʾ��

(1)�÷�ӦΪ���淴Ӧ����800 ��ʱ����CO����ʼŨ��Ϊ2.0 mol��L-1��ˮ��������ʼŨ��Ϊ3.0 mol��L-1���ﵽ��ѧƽ��״̬���CO2��Ũ��Ϊ1.2 mol��L-1����˷�Ӧ��ƽ�ⳣ��Ϊ___�������¶����߸÷�Ӧ�Ļ�ѧƽ�ⳣ���ı仯������___�������������������С��������������
(2)ij�¶��£��÷�Ӧ��ƽ�ⳣ��ΪK=1/9�����¶����ڼס��ҡ������������ܱ�������Ͷ��H2O(g)��CO(g)������ʼŨ�����±���ʾ�������жϲ���ȷ����____(����ĸ)��
��ʼŨ�� | �� | �� | �� |
c(H2O)/mol��L-1 | 0.010 | 0.020 | 0.020 |
c(CO)/mol��L-1 | 0.010 | 0.010 | 0.020 |
A. ��Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
B. ƽ��ʱ�����кͱ���H2O��ת���ʾ���25%
C. ƽ��ʱ������c(CO2)�Ǽ��е�2������0.015 mol��L-1
D. ƽ��ʱ������H2O��ת���ʴ���25%
(3)һ�������£����淴ӦN2(g)+3H2(g)![]() 2NH3(g)����H<0���ﵽƽ���
2NH3(g)����H<0���ﵽƽ���
�ټӴ�����v(��)��v(��)�������仯���ұ仯�ı���__(��������������������)��
����С���ʹ��ϵѹǿ������v(��)___��v(��)___(����������������С������������)��v(��)�仯�ı���__v(��)�仯�ı���(��������������С��������������)��
�۽��£�v(��) ____��v(��)__(����������������С������������)��
���º�ѹ����ͨ��һ������He���ﵽ��ƽ��ʱ��N2��ת����__��c(H2)��__(����������������С������������)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com