
甲、乙两同学进行课外实验,各取250 mL无色透明饮料瓶一个,依次加入4 g氢氧化钠、4 g葡萄糖、半瓶水、3滴0.2%的亚甲基蓝溶液旋上瓶塞振荡,溶液呈蓝色,静置后溶液变为无色。甲再次振荡,又呈蓝色,静置后又变为无色,多次反复可重现上述现象。而乙在蓝色消失后,向瓶内加满水旋上瓶塞,振荡却不再出现蓝色,乙认为是物质浓度不同引起的。甲设计并完成了一个实验,否定了乙的说法。
你认为甲实验的操作和现象是________________。振荡后出现的蓝色主要与________有关(填写化学式,下同);蓝色消失又与________有关。
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
下图中A、B、C、D、E、F、G均为有机化合物。
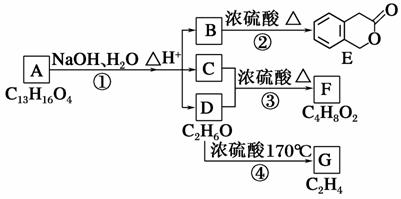
根据图示回答问题:
(1)D的化学名称是________。
(2)反应③的化学方程式是________(有机物用结构简式表示)。
(3)B的分子式是________,A的结构简式是________,反应①的反应类型是________。
(4)符合下列3个条件的B的同分异构体的数目有________个。
①含有邻二取代苯环结构
②与B有相同官能团
③不与FeCl3溶液发生显色反应
写出其中任意一个同分异构体的结构简式________。
(5)G是重要的工业原料,用化学方程式表示G的一种重要的工业用途________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用四种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A. | 通入CO2,溶液变浑浊 | CaCl2溶液 |
| B. | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C. | 通入CO2,溶液变浑浊。再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| D. | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊 | Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于实验室一般事故的预防和处理方法正确的是( )
A.燃着的酒精灯打翻失火,应立即用水浇灭
B.少量酸或碱滴到实验台上,立即用湿抹布擦净,再用水冲洗
C.金属镁着火时,可用干冰灭火器来扑灭
D.蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
右表为元素周期表前四周期的一部分,下列有关
 W、X、Y、Z四种元素的叙述中,正确的是
W、X、Y、Z四种元素的叙述中,正确的是
A.与氢原子形成的化学键的键能:W比Y的大
B.与氢原子形成的化学键的极性:X比Y的弱
C.最低价气态氢化物的沸点:X的比W的高
D.XZ3的晶体属于离子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备纳米颗粒Y(化合物)的反应为:
3Fe2++2S2O32-+O2+4OH-===Y+S4O62-+2H2O,下列有关说法正确的是
A.Y的化学式为Fe2O3
B.S4O62- 是还原产物
C.被1mol O2氧化的Fe2+物质的量为1 mol
D.每 32 gO2参加反应,转移电子的物质的量为4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合气体中可能含有 Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是( )
A.肯定有SO2,但无NO
B.肯定没有Cl2、O2和NO2
C.可能有Cl2和O2
D.肯定只有NO
查看答案和解析>>
科目:高中化学 来源: 题型:
 I是常规核裂变产物之一,可以通过测定大气或水中
I是常规核裂变产物之一,可以通过测定大气或水中 I的含量变化来监测核电站是否发生放射性物质泄漏。下列有关
I的含量变化来监测核电站是否发生放射性物质泄漏。下列有关 I的叙述中错误的是( )
I的叙述中错误的是( )
A. I的化学性质与
I的化学性质与 I相同
I相同
B. I的原子序数为53
I的原子序数为53
C. I的原子核外电子数为78
I的原子核外电子数为78
D. I的原子核内中子数多于质子数
I的原子核内中子数多于质子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com