
某研究性学习小组通过测量镁铝合金和盐酸反应生成气体体积的方法来测定合金的成分,他们取10.2g镁铝合金与盐酸恰好完全反应,反应后收集到11.2L氢气(标准状况),试求:
(1)反应过程中消耗盐酸的物质的量
(2)10.2g合金中镁的质量。(请写出具体的计算过程)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:推断题
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化为烃B、烃C。以C为原料可以合成聚对羟基苯甲酸 (G)。已知:
(1) A是一种有机酸,分子式为C9H10O3。
(2)B的相对分子质量为104,分子中含苯环且能使溴的四氯化碳溶液褪色。
(3) C的相对分子质量为78,且分子中只有一种氢原子。
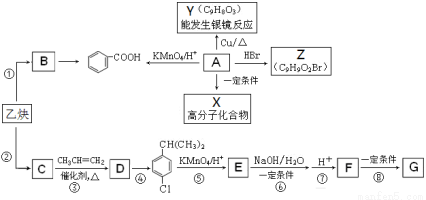
(1)写出乙炔分子的电子式____________, F中的含氧官能团名称_____________;
(2)上述①至⑧的反应中,属于加成反应的有____________,
(3)写出A的结构简式____________;
(4)下列有关的描述中,正确的是__________;
a. 1molB最多能与4molH2加成
b. B通过氧化反应可使溴水和酸性KMnO4溶液褪色
c. B、C、D是同系物
d. A→X的反应属于缩聚反应
(5)写出A→Y反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上期中测试化学试卷(解析版) 题型:选择题
已知单位体积的溶液中,难挥发性溶质的分子或离子数越多,该溶液的沸点越高,则下列溶液的沸点最高的是
A.2L 0.01mol/L的蔗糖溶液
B.2L 0.01mol/L的CaCl2溶液
C.1L 0.02mol/L的NaCl溶液
D.1L 0.02mol/L的CH3COOH溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏中卫一中高二上第四次月考化学试卷(解析版) 题型:选择题
等体积的盐酸和醋酸分别和等量的锌反应,已知反应开始时速率相等,反应结束后两种酸均有剩余,下列判断中不正确的是
A.反应前两种酸的物质的量浓度不同
B.反应开始后,盐酸的H+浓度减小快
C.反应开始后,两种酸产生的氢气量相同
D.从反应开始到结束,醋酸所用的时间较少
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏中卫一中高二上第四次月考化学试卷(解析版) 题型:选择题
100℃,Kw=1.0×10-12,若在此温度时,某溶液中的c(H+)=1.0×10-7 mol•L-1,则该溶液
A.呈中性 B.呈碱性
C.呈酸性 D.1000c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏中卫一中高一上第三次月考化学试卷(解析版) 题型:选择题
金属加工后的废切削液中含2%~3%的NaNO2,它是一种环境污染物,人们用NH4Cl溶液来处理废切削液,使NaNO2转化为无毒物质,该反应分两步进行:
第一步:NaNO2+NH4Cl=NaCl+NH4NO2
第二步:NH4NO2=N2↑+2H2O
下列对第二步反应的叙述中正确的是
①NH4NO2只是氧化剂 ②NH4NO2只是还原剂
③NH4NO2发生了分解反应 ④只有氮元素的化合价发生了变化
⑤NH4NO2既是氧化剂又是还原剂
A.①③ B.①④ C.②③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏中卫一中高一上第三次月考化学试卷(解析版) 题型:选择题
下列溶液中溶质的物质的量浓度为1mol/L的是
A.将40gNaOH溶解于1L水中配成的NaOH溶液
B.常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液
C.从1000mL1mol/LNaCl溶液中取出100mL的溶液
D.将VL0.5mol/L的浓盐酸加热浓缩为V/2L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高一上期中测试化学试卷(解析版) 题型:选择题
根据下列反应:2Fe3++2I-=2Fe2++I2,Br2+2Fe2+=2Br-+2Fe3+,判断微粒的氧化性从强到弱的顺序是( )
A.Fe3+、Br2、I2 B.I2、Br2、Fe3+ C.Br2、Fe3+、I2 D.Br2、I2、Fe3+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高一上期中测试化学试卷(解析版) 题型:实验题
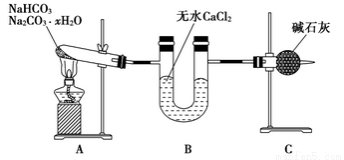
现有NaHCO3和Na2CO3·xH2O的混合物,为了测定x值,某同学采用如图所示的装置进行实验(CaCl2、碱石灰均足量)。
已知:①2NaHCO3  Na2CO3 + CO2↑+ H2O ②含结晶水的物质加热易失去结晶水
Na2CO3 + CO2↑+ H2O ②含结晶水的物质加热易失去结晶水
(1)B装置的作用是_________________________
(2)C装置的作用是_________________________
(3)若在装置A的试管中装入NaHCO3和Na2CO3·xH2O的混合物3.7 g,用酒精灯加热到反应完全及A、B、C装置的质量不再发生变化,此时B管增重1.89 g,C管增重0.22 g,则x的值为________________
(4)该装置还不是很完善,可能使测定结果偏小,应如何改进 __________,原因为________________
(5)有同学认为,也可以用以下方案测出x值:取一定质量NaHCO3和Na2CO3·xH2O的混合物(混合物质量为m1),使之与足量盐酸反应,产生的气体经浓硫酸干燥后用碱石灰吸收(HCl、空气等干扰因素已排除),测出碱石灰增重质量为m2。请判断该方案是否可行(选填①或②,若同时作答,不得分)
①若可行,请写出x值计算表达式
②若不可行,如果补做以下哪个实验就可算出x值 (不定项选择)
A.另取相同质量的混合物,加热至质量不再减少,测出剩余固体的质量
B.测出该方案中浓硫酸的增重质量
C.把与盐酸反应后的溶液蒸干,测出所得固体的质量
D.另取相同质量的混合物,加水溶解,加入足量Ba(OH)2溶液,过滤、洗涤、干燥,测出滤渣的质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com