
下列实验方案中,合理的是
A.可用生石灰除去乙酸中少量水
B.用5 mL苯与1mL浓溴水反应(Fe粉作催化剂)制溴苯
C.向适量浓硝酸、浓硫酸的混合物中逐滴加入苯,在50~60℃的水浴中加热以制取硝
基苯
D.将2.5g苯酚、2.5mL40%的甲醛溶液混合,沸水浴加热制酚醛树脂
科目:高中化学 来源: 题型:
下列中学化学中常见物质的转化关系如图,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物.
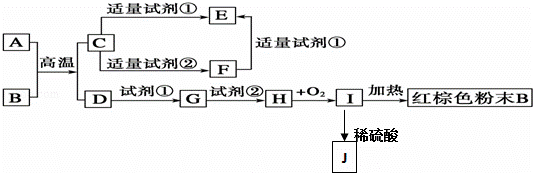
(1)写出B的化学式 ;
(2)写出反应A+B→C+D的一种应用 ;
(3)写出过量的D与稀硝酸反应的离子方程式: ;
(4)H→I的化学方程式: ;
(5)某同学认为物质J 中可能同时含有同一金属元素的不同价态,若要确定其中低价阳离子的存在最好应选用 ;
A、KSCN溶液和氯水 B、铁粉和KSCN 溶液C、浓氨水 D、KMnO4溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下列实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤作用的活性物质。
下列说法错误的是( )
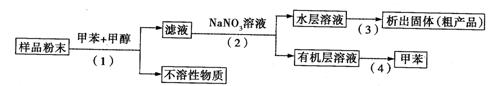
A.步骤(1)需要过滤装置 B.步骤(3)需要用到蒸发皿
C.步骤(4)是利用物质的沸点差异进行分离的
D.活性物质易溶于有机溶剂,难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
纸层析法分离铁离子和铜离子的实验中,正确的操作是
A.在滤纸上点样时,试样点以稍大为宜
B.应沿试管壁小心地将展开剂慢慢倒入试管底部
C.将滤纸上的试样点浸入展开剂中
D.点样后的滤纸需晾干后,才能将其浸入展开剂中
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,
反应的化学方程式如下:
2NH3(g)+CO2(g)  NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用右图装置制取氨气,你所选择的试剂是 。

(2)制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
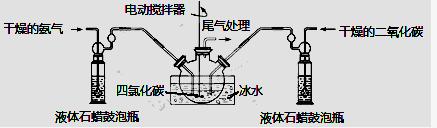
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是: 、 。液体石蜡鼓泡瓶的作用是: 。
②从反应后的混合物中分离出产品,为了得到干燥产品,应采取的方法是_______ (填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
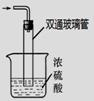
③尾气处理装置如右图所示。双通玻璃管的作用: ;
浓硫酸的作用: 、 。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品11.73 g,用足量石灰水 充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为15.00 g。则样品中氨基甲酸铵的物质的量分数为 。
[Mr(NH2COONH4)=78g/mol、Mr(NH4HCO3) =79 g/mol、Mr(CaCO3)=100 g/mol]【来.源:全,
查看答案和解析>>
科目:高中化学 来源: 题型:
卤素单质及其化合物在生产和生活中有广泛应用。
Ⅰ、氟化钠主要用作农作物杀菌剂、杀虫剂、木材防腐剂。实验室以氟硅酸(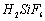 )等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:
)等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:
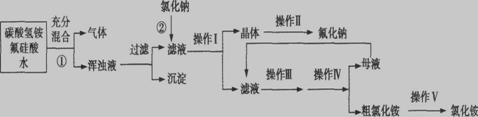
已知:20℃时氯化铵的溶解度为37.2 g,氟化钠的溶解度为4 g,Na2SiF6微溶于水。
请回答下列有关问题:
(1)完成并配平上述流程中①、②的化学反应方程式:

② 。
(2)操作Ⅲ分为两步,其顺序是 (填写所选序号)。
a、过滤 b、加热浓缩 c、冷却结晶 d、洗涤
操作Ⅱ是洗涤、干燥,其目的是 ,在操作Ⅰ~V中与之相同的操作步
骤是 。
(3)流程①中NH4HCO3必须过量,其原因是 。
Ⅱ、紫菜与海带类似,是一种富含生物碘的海洋植物,可用于食用补碘。以下为某兴趣小组模拟从紫菜中提取碘的过程:
 已知:商品紫菜轻薄松脆,比海带更易被焙烧成灰(此时碘转化为碘化物无机盐)。
已知:商品紫菜轻薄松脆,比海带更易被焙烧成灰(此时碘转化为碘化物无机盐)。
(4)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式:
。
(5)操作①中涉及两步操作,名称是 ,所用的主要玻璃仪器为 ,所用试剂A最好选用表格中的 (填试剂名称)。
| 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) | |
| 密度/g、cm-3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |
(6)将下列装置图中缺少的必要仪器补画出来,以最终将单质碘与试剂A分离:

查看答案和解析>>
科目:高中化学 来源: 题型:
下图中A、B、C、D、E、F、G均为有机化合物。根据下图回答下列问题。

(1)D的化学名称是__________。
(2)反应③的化学方程式是________________________________。
(有机物须用结构简式表示)
(3)B的分子式是____________;A的结构式是______________;反应①的反应类型是____________。
(4)符合下列3个条件的B的同分异构体的数目有______种。
(Ⅰ)为邻位取代苯环结构;(Ⅱ)与B具有相同官能团;
(Ⅲ)不与FeCl3溶液发生显色反应。
写出其中任意一种同分异构体的结构简式____________________________________。
(5)G是重要的工业原料,用化学方程式表示G的一种重要的工业用途
_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
多昔芬主要用于防治骨质疏松等病症,其合成路线如下:
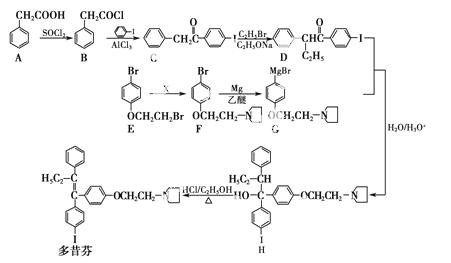
说明:D+G—→H的转化中分别发生了加成反应和水解反应。
(1)D中含 氧官能团的名称是________。
氧官能团的名称是________。
(2)C→D的反应类型是________,H→多昔芬的反应类型是________。
(3)E→F转化中另一产物是HBr,则试剂X的结构简式是________。
(4)H分子中有________个手性碳原子。
(5)写出同时满足下列条件的A物质同分异构体的结构简式:________。
①能发生银镜反应 ②与FeCl3发生显色反应 ③苯环上的一溴代物只有2种
(6) 苯甲酰氯(
苯甲酰氯(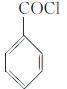 )是合成药品的重要中间体。请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
)是合成药品的重要中间体。请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
CH2===CH2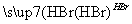 CH3CH2Br
CH3CH2Br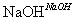 CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
已知,在450℃并有催化剂存在下进行如下反应:
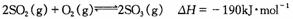
(1)硫酸工业中,该反应需要通入过量空气的目的是 ;该反应不在更高温度下进行的原因是 。
(2)在容积固定的密闭容器中,下列情况已达到平衡状态的是 。
A.v(O2)正=2v(SO3)逆 B.容器中气体的压强不随时间而变化
C.容器中气体的密度不随时间而变化 D.容器中气体的原子总数不随时间而变化
(3)当向上述平衡体系中通入18O2气体,再次达到平衡时,18O存在于 中。
A. SO2、O2 B.SO2、SO3 C.SO3 D.SO2、SO3、O2
(4)在一个固定容积为2L的密闭容器中充入0.20 mol SO2和0.10mol O2,在450℃并有催化剂条件下,2分钟后达到平衡,测得容器中含SO30.16mol,则
v(O2)= mol( L·min-1);放出的热量为 kJ;该温度下的平衡常数为 ;若继续通入0.20mol SO2和0.10mol O2,则再次平衡时,二氧化硫的转化率 (选填“变大”或“变小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com