
【题目】草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液。将25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定到KMnO4不再褪色为止。
试回答:
(1)实验中不考虑铁架台等夹持仪器外,不需要的仪器有(填序号) ,还缺少的仪器有(填名称)_ 。
A托盘天平(带砝码,镊子) B滴定管 C 100mL容量瓶 D烧杯
e.漏斗 f.锥形瓶 g.玻璃棒 h.烧瓶
(2)实验中,标准液KMnO4溶液应装在______________式滴定管中。
(3)若在滴定前没有用amol·L-1的KMnO4溶液对滴定管进行润洗,则所测得的x值会___________(偏大、偏小、无影响)。
(4)在滴定过程中若用amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为__________mol·L-1,由此可计算x的值是____________。
(5)写出酸性高锰酸钾溶液滴定草酸溶液过程中反应的离子方程式_______________。
【答案】(1)eh 胶头滴管
(2)酸 (3)偏小
(4)0.1av (w-0.9av)/0.18av
(5)2MnO4-+ 5H2C2O4+6H+=2Mn2++10CO2↑+ 8H2O
【解析】
试题分析:(1)实验不需要过滤,不用漏斗;不用蒸馏,不需要烧瓶;配制溶液定容时用胶头滴管;(2)高锰酸钾溶液具有氧化性,标准液KMnO4溶液应装在酸式式滴定管中;(3)若在滴定前没有用amol·L-1的KMnO4溶液对滴定管进行润洗,则标准液浓度降低,消耗标准液体积偏大,则草酸的物质的量偏大,草酸晶体的摩尔质量偏小,所测得的x值会偏小;
(4)
x=![]()
c=![]() ÷0.025L=0.1av
÷0.025L=0.1av
设草酸晶体的摩尔质量是M,![]() ,
,
![]() ,
,![]() ,x=(w-0.9av)/0.18av;
,x=(w-0.9av)/0.18av;
(5)酸性高锰酸钾溶液与草酸溶液反应的离子方程式2MnO4-+ 5H2C2O4+6H+====2Mn2++10CO2↑+ 8H2O。


科目:高中化学 来源: 题型:
【题目】如图所示,通电5 min时:第③极增重2.16 g,并且观察到A池中只有一个电极在产生气体,通电5min后 ,A池两极均有气体产生。设A池中原混合液的体积为200 mL,求
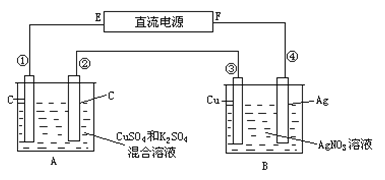
(1)直流电源E是________极;
(2)通电前A池中原混合溶液Cu2+的浓度____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用漂白粉溶液浸泡过的有色布条,如果晾置在空气中,过了一段时间,其漂白效果会更好的原因可能是
A. 漂白粉被氧化了
B. 有色布条被空气中的氧气氧化了
C. 漂白粉溶液跟空气中的CO2的反应充分,生成了较多量的次氯酸
D. 漂白粉溶液蒸发掉部分水,其浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属腐蚀的电化学原理可用下图模拟。

(1)请写出有关电极反应式:_________________________
①铁棒上的电极反应式:_______________________
碳棒上的电极反应式:_________________________
(2)该图所表示的是_________________________(填“析氢”或“吸氧”)腐蚀。
(3)若将O2撤走,并将NaCl溶液改为稀H2SO4溶液,则此图可表示__________(填“析氢”或“吸氧”)腐蚀原理;若用牺牲阳极法来保护铁棒不被腐蚀溶解,即可将碳棒改为_________棒。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在其它条件一定时,图中曲线表示反应2NO(g)+ O2(g) ![]() 2NO2(g) △H>0达平衡时NO 的转化率与温度的关系,图上标有A、B、C、D、E点,下列有关说法正确的是( )
2NO2(g) △H>0达平衡时NO 的转化率与温度的关系,图上标有A、B、C、D、E点,下列有关说法正确的是( )
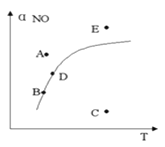
A.A点反应未达到平衡状态,且反应正向移动
B.C点NO转化率最低,且化学反应速率最小
C.B、D两点均处于相应温度下的化学平衡状态,且αB(NO)<αD(NO)
D.E点反应未达平衡,反应正向移动,容器内压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀。根据上述实验事实,下列说法中,不正确的是
A.溶解度 MnS<PbS
B.MnS存在沉淀溶解平衡 MnS(s)![]() Mn2+(aq) + S2-(aq)
Mn2+(aq) + S2-(aq)
C.Cu2+转化为沉淀的原理为 MnS(s) + Cu2+(aq)=CuS(s) + Mn2+(aq)
D.沉淀转化能用于除去溶液中的某些杂质离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )

A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C. 离子Y2﹣和Z3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在xR2++yH++O2═mR3++nH2O的离子方程式中,对系数m和R3+的判断正确的是( )
A.m=4,R3+是氧化产物
B.m=n,R3+是氧化产物
C.m=2,R3+是还原产物
D.m=y,R3+是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com