
| A.KNO3溶液 | B.NaCl溶液 | C.铜粉 | D.硫酸铜晶体 |
科目:高中化学 来源:不详 题型:单选题
| A.化学反应速率是表示化学反应快慢的物理量 |
| B.一般情况下,升高温度能加快化学反应速率 |
| C.可逆反应达到化学反应限度时,反应就静止不动了 |
| D.可逆反应达到化学反应限度时,正反应速率等于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
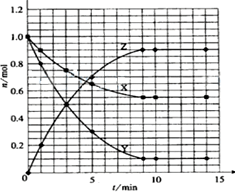
A.反应的化学方程式是X+2Y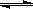 2Z 2Z |
| B.该反应在0-3min时间内产物Z的平均反应速率0.083mol·L-1·min-1 |
| C.在3分钟时Y和Z的浓度相等 |
| D.其他条件不变,升高温度,若正反应速 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 CH3OH(g),经过5分钟后达到平衡状态,若此时测得CH3OH蒸汽的浓度为2mol/L,求:
CH3OH(g),经过5分钟后达到平衡状态,若此时测得CH3OH蒸汽的浓度为2mol/L,求:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增加反应物的用量,化学反应速率一定加快 |
| B.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
| C.pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强 |
| D.将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为碳酸钠 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加热一般能加快化学反应速率 |
| B.粉碎固体物质能加快化学反应速率 |
| C.不同物质的化学反应速率可能不一样 |
| D.化学方程式中各物质的化学反应速率之比等于其质量比 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 I.合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
I.合成氨工业对国民经济和社会发展具有重要的意义。其原理为: (g)
(g)  2NH3(g) △H=" -92.4" kJ/mol 据此回答以下问题:
2NH3(g) △H=" -92.4" kJ/mol 据此回答以下问题: 2NH3(g),下列哪种情况下,
2NH3(g),下列哪种情况下,| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入NH3的物质的量 |
| y | NH3的物质的量 | 平衡常数K | NH3的转化率 | 生成物物质的量总和 |
| | 0.01mol·L-1 KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol·L-1 Na2SO3溶液的体积/mL | H2O的体积 /mL | 实验 温度 /℃ | 溶液出现蓝色时所需时间/s |
| 实验1 | 5 | V1 | 35 | 25 | --------- |
| 实验2 | 5 | 5 | 40 | 25 | ---------- |
| 实验3 | 5 | 5 | V2 | 0 | ----------- |
 H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率
H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率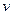 与时间t的关系如右图。
与时间t的关系如右图。 ;
;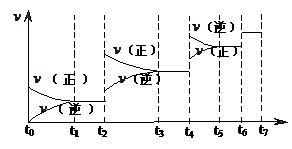
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3的反应中,在5s中NH3的浓度变化了8mol/L。则NH3的平均反应速率
2NH3的反应中,在5s中NH3的浓度变化了8mol/L。则NH3的平均反应速率| A.2.4 mol/(L·s) | B.0.8mol/(L·s) | C.1.6 mol/(L·s) | D.0.08 mol/(L·s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com