
| A. | 100mL的该溶液中含3.28g溶质 | |
| B. | .500mL的该溶液中含0.2molNO3- | |
| C. | 600mL的该溶液中Ca2+与NO3的物质的量浓度之比是1:2 | |
| D. | .800nmL的该溶液中NO3-的总浓度为3.2mol•L-1. |
分析 A.溶质物质的量n=cV=$\frac{m}{M}$计算分析;
B.溶质物质的量n=cV,离子物质的量=溶质物质的量×离子个数;
C.离子浓度=溶质浓度×离子数;
D.溶液中离子浓度和溶液体积无关,溶液是均一稳定的.
解答 解:A.100mL0.2mol•L-1的Ca(NO3)2溶液中含溶质质量=0.2mol/L×0.1L×164g/mol=3.28g,故A正确;
B.溶质物质的量n=cV=0.5L×0.2mol/L=0.1mol.则500mL的该溶液中含0.2molNO3-,故B正确;
C.600mL0.2mol•L-1的该溶液中Ca2+与NO3的物质的量浓度之比是1:2,故C正确;
D.800nmL的该溶液中NO3-的总浓度=0.2mol/L×2=0.4mol/L,故D错误.
故选D.
点评 本题考查了有关物质的量浓度的计算,题目难度不大,注意掌握物质的量浓度的概念及计算方法,明确化学式与离子的关系是解本题的关键.


科目:高中化学 来源: 题型:选择题
| A. | Mg2+、K+、SO42-、OH- | B. | Na+、Ag+、NO3-、Cl- | ||
| C. | H+、Ba2+、NO3-、Cl- | D. | Ca2+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CO18OH与CH3OH发生酯化反应达到平衡后,18O仅存在于乙酸、水分子里 | |
| B. | 在体积可变的密闭容器中在一定条件下2molSO2和2molO2发生反应:2SO2(g)+O2═2SO3(g),达到反应最大限度时,容器体积变为反应前的81.25%,则SO2转化率为70% | |
| C. | 对于任何化学反应来说,反应速率越快,反应现象不一定就越明显 | |
| D. | 某同学在用锌片与稀硫酸反应制取氢气时,向反应器中加入少量CuSO4固体(不考虑温度变化),则此时产生H2的化学反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 )广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精.已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下:
)广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精.已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下: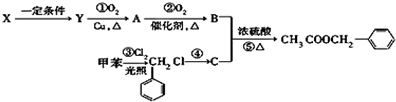
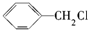 发生反应④所需的条件是氢氧化钠水溶液、加热,该反应的反应类型为水解反应.
发生反应④所需的条件是氢氧化钠水溶液、加热,该反应的反应类型为水解反应.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com