
| A. | 10个 | B. | 20个 | C. | 40个 | D. | 80 |
分析 乙醛与银之间的关系式为CH3CHO~2Ag,根据关系式计算出生成银的物质的量,然后根据m=nM计算出银的质量,最后根据“生产一个暖瓶胆需0.54gAg”计算出最多可以制得暖瓶胆的数目.
解答 解:根据关系式CH3CHO~2Ag可知,0.05mol乙醛完全反应生成银的物质的量为:0.05mol×2=0.1mol,生成银的质量为:108g/mol×0.1mol=10.8g,
则最多可以制得暖瓶胆的数目为:$\frac{10.8g}{0.54g}$=20,
故选B.
点评 本题考查了化学方程式的计算,题目难度不大,明确发生反应的实质为解答关键,注意掌握常见有机物结构与性质,试题培养了学生的化学计算能力.


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:选择题
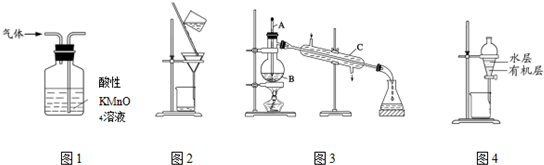
| A. | 用图1所示装置可除去甲烷中乙烯杂质 | |
| B. | 用图2所示装置分离硫酸铜溶液和铜 | |
| C. | 用图3所示装置分离乙醇和水 | |
| D. | 用图4所示装置分离苯萃取碘水后已分层的有机层和水层 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:选择题
在一密闭容器中,反应aA(g) 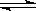 bB(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向正反应方向移动了
B.物质A的转化率增大了
C.物质B的质量分数增加了
D.a >b
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
在标准状况下,mg气体A与ng气体B的分子数相同,下列说法中不正确的是( )
A.两种气体A与B的相对分子质量之比为m:n
B.同质量气体A与B的分子数之比为n:m
C.同温同压下,A、B两气体的密度之比为n:m
D.相同状况下,同体积A、B两气体的质量之比为m:n
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
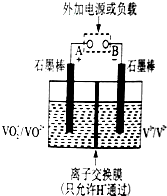 钒(V)及其化合物在工业催化、新材料和新能源等领域中有广泛的应用.回答下列问题:
钒(V)及其化合物在工业催化、新材料和新能源等领域中有广泛的应用.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

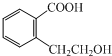
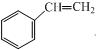
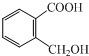
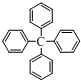
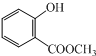
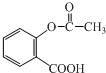
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
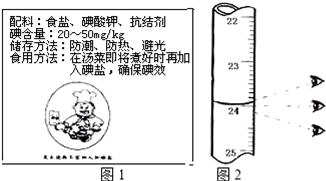
| 编号 | 碱式滴定管读数 | 消耗体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 0 | 如图一 | |
| 2 | 0 | 23.97 | 23.97 |
| 3 | 0 | 24.03 | 24.03 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com