
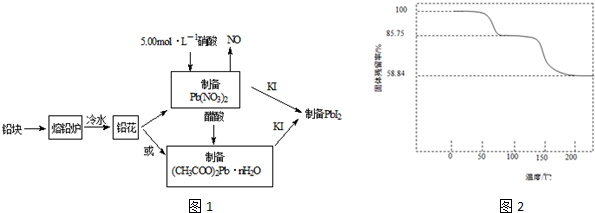
分析 (1)铅块制成铅花为了增大表面积,根据影响反应速率的因素去分析;
(2)铅溶解于稀硝酸的反应方程式为3Pb+8HNO3=3Pb(NO3)2+2NO+4H2O,根据溶解的铅的物质的量可计算消耗的硝酸溶液及生成NO的体积;
(3)①可假设起始固体质量为100g,则加热到75℃时完全失去结晶水的质量就是固体减轻的质量,求算出水的物质的量及醋酸铅的物质的量,根据两者的物质的量之比可确定n的值;
②醋酸铅继续加热分解剩余固体为铅的氧化物,可根据剩余固体质量及铅、碳原子守恒来确定有机物的摩尔质量,推测有机物的分子组成;
(4)根据酸碱中和的原理可计算出溶液中的H+的浓度,并结合关系式确定溶液里Pb2+的浓度,再计算Ksp.
解答 解:(1)将铅块制成铅花,是为了增大与酸反应的接触面积,加快溶解反应速率,
故答案为:增大与酸的接触面,加快溶解反应速率;
(2)31.05g铅的物质的量为$\frac{31.05g}{207g/mol}$=0.15mol,根据反应方程式可知消耗的HNO3的物质的量为0.15mol×$\frac{8}{3}$=0.4mol,生成的NO的物质的量为0.15mol×$\frac{2}{3}$=0.1mol,则硝酸溶液的体积为0.4mol÷5.00mol•L-1=0.08L=80.0mL,生成NO的体积为0.1mol×22.4L/mol=2.24L,
故答案为:80.0;2.24;
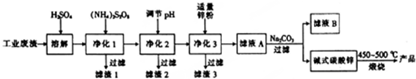
(3)①假设样品的起始质量为100克,根据固体残留率的公式可知,75℃时剩余固体为87.75克,生成的水质量为100g-87.75g=12.25g,则醋酸铅与水的物质的量之比为$\frac{85.75g}{325g/mol}$:$\frac{12.25g}{18g/mol}$=1:3,则n=3,
故答案为:3;
②铅的氧化物质量为58.84克,醋酸铅的物质的量为=$\frac{85.75g}{325g/mol}$=$\frac{85.75}{325}$mol,根据铅原子守恒,铅的氧化物(PbOx)的物质的量为=$\frac{85.75}{325}$mol,此氧化物的摩尔质量为58.84g÷=$\frac{85.75}{325}$mol=223g/mol,为PbO,有机物的质量为85.75g-58.84g=26.91g,此有机物分子内应含有四个碳原子,物质的量为=$\frac{85.75}{325}$mol,摩尔质量为26.91g÷=$\frac{85.75}{325}$mol=102,根据原子守恒可知有机物的分子式为C4H6O3,结构简式为(CH3CO)2O,
故答案为:(CH3CO)2O;
(4)n(H+)=n(NaOH)=0.002500 mol•L-1×20.00mL×10-3L•mL-1=5.000×10-5mol,
n[Pb2+(aq)]=$\frac{1}{2}$n(H+)=2.500×10-5mol,
c(Pb2+)=$\frac{2.500×10{\;}^{-5}mol}{25.00mL×10{\;}^{-3}L/mL}$=1.000×10-3 mol•L-1
Ksp(PbI2)=c(Pb2+)•c2(I-)=4c3(Pb2+)=4×(1.000×10-3)3=4.000×10-9,
答:室温时PbI2 的Ksp 为4.000×10-9.
点评 本题以制备碘化铅为载体,重点考查学生的数据处理能力,难度较大,对学生的分析问题,解决问题的能力要求较高,建议适当训练类似题目.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Al(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.7 | 7.5 | 5.4 | 4.0 | 6.4 |
| 完全沉淀时的pH | 3.7 | 9.5 | 6.6 | 5.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn、Fe | B. | Fe、Mg | C. | Al、Mg | D. | Zn、Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com