

 H3O2++HO2-,
H3O2++HO2-, H3O2++HO2-;
H3O2++HO2-;| 256kJ |
| 0.4 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | A1(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 键能的大小可以衡量化学键的强弱,参考以下表格的键能数据,回答下列问题:
键能的大小可以衡量化学键的强弱,参考以下表格的键能数据,回答下列问题:| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不能透过滤纸 |
| B、有丁达尔效应产生 |
| C、所得液体一定无色透明 |
| D、不稳定、很快会分层 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MnO2 |
| B、KMnO4溶液 |
| C、稀盐酸 |
| D、Na2SO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
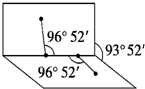 已知H2O2的结构如图:H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O-H键与O-O键的夹角均为96°52′,试回答:
已知H2O2的结构如图:H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O-H键与O-O键的夹角均为96°52′,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
A、过氧化钠的电子式: | ||
B、质子数为35、中子数为45的溴原子:
| ||
C、硫离子的结构示意图: | ||
D、间二甲苯的结构简式: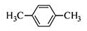 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、甲基的电子式: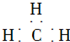 | ||
B、镁离子的结构示意图: | ||
C、质量数为34、中子数为18的核素:
| ||
D、乙酸的结构简式: |
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省宿迁市五校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列反应中,都有水参加,其中水既不作氧化剂,又不作还原剂的氧化还原反应是
A.2Na+2H2O=2NaOH+H2↑
B.Na2O+H2O=2NaOH
C.Cl2+H2O=HCl+HClO
D.NaH+H2O=NaOH+H2↑(NaH中H为-1价)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com