
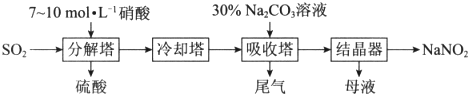
分析 (1)吸收塔中发生的是氮的氧化物被碳酸钠溶液吸收的化学反应,化学方程式是NO+NO2+Na2CO3=2NaNO2+CO2↑;
(2)分解塔中需要严格控制硝酸的浓度,是使二氧化硫与硝酸反应产生一氧化氮和二氧化氮的量之比为1:1,便于的吸收塔中恰好转化为亚硝酸盐;
(3)反应产生的一氧化氮可通过氧化,将部分转化为二氧化氮,然后通入吸收塔中循环利用.
解答 解:(1)一氧化氮和二氧化氮被碳酸钠溶液吸收,反应的方程式为NO+NO2+Na2CO3=2NaNO2+CO2↑,故答案为:NO+NO2+Na2CO3=2NaNO2+CO2↑;
(2)分解塔中需要严格控制硝酸的浓度,是使二氧化硫与硝酸反应产生一氧化氮和二氧化氮的量之比为1:1,便于的吸收塔中恰好转化为亚硝酸盐,所以目的是控制产物中NO和NO2的比例,故答案为:控制产物中NO和NO2的比例;
(3)反应产生的一氧化氮可通过氧化,将部分转化为二氧化氮,然后通入吸收塔中循环利用,故答案为:回收,补充适量O2后,通入吸收塔中循环利用.
点评 本题考查了工业制备原理应用,流程分析,实验制备物质的分析判断,明确转化中的化学反应得出物质之间的关系是解答的关键,题目难度中等.


科目:高中化学 来源: 题型:实验题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水蒸发制海盐的过程只发生化学变化 | |
| B. | 只通过物理变化即可从海水中提取溴单质 | |
| C. | 从海水中可以得到MgCl2,可电解MgCl2溶液制备Mg | |
| D. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
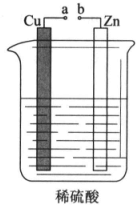 课外小组的同学对如图所示的实验装置进行了研究.
课外小组的同学对如图所示的实验装置进行了研究.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只可能是① | B. | 只可能是③ | C. | 可能是①或③ | D. | 可能是①或②或③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com