
| A.在接触室中使用铁粉作催化剂 |
| B.在接触室中运用热交换技术可充分利用能源 |
| C.把硫铁磨成细粉末,可以提高原料的利用率 |
| D.该反应采用450~500℃主要是因为该温度下催化剂活性好 |
 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

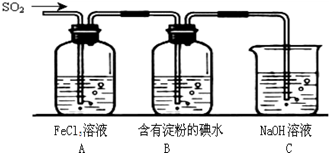
| A.烧瓶 | B.酒精灯 | C.漏斗 | D.烧杯 E.玻璃棒 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.点燃硫磺.产生刺激性气味气体,该气体可以漂白纸浆 |
| B.向蔗糖中加入浓硫酸,蔗糖变黑色,说明浓硫酸具有强的吸水性 |
| C.将H2S气体通入CuSO4溶液生成CuS沉淀,说明H2S为强电解质 |
| D.将Al片加入浓硫酸中,反应剧烈,说明浓硫酸具有强的氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
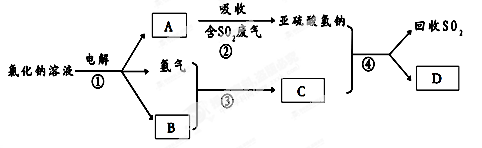
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )| A.BaSO3和BaSO4 | B.BaS | C.BaSO3 | D.BaSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无法确定样品中钠、硫元素的质量比 |
| B.Na2SO3已被氧化 |
| C.加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 |
| D.加入稀硝酸后的沉淀一定是BaSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜与浓硫酸反应所得白色固体不是CuSO4 |
| B.加BaCl2溶液后所得白色沉淀是BaSO3 |
| C.白色固体中夹杂的少量黑色物质可能是CuO |
| D.白色固体中夹杂的少量黑色物质中一定含有元素Cu和S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
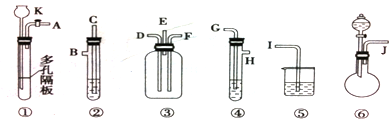
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com