
”¾ĢāÄæ”æČżŃĪ»łĮņĖįĒ¦(3PbO”¤PbSO4”¤H2O£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ990)¼ņ³Ę”°ČżŃĪ”±£¬²»ČÜÓŚĖ®¼°ÓŠ»śČܼĮ”£Ö÷ŅŖŹŹÓĆÓŚ²»ĶøĆ÷µÄ¾ŪĀČŅŅĻ©Ó²ÖŹ¹Ü”¢×¢Éä³ÉŠĶÖĘĘ·£¬Ņ²æÉÓĆÓŚČĖŌģøļµČČķÖŹÖĘĘ·”£ŅŌĒ¦Äą (Ö÷ŅŖ³É·ÖĪŖPbO”¢Pb¼°PbSO4µČ)ĪŖŌĮĻÖʱøČżŃĪµÄ¹¤ŅÕĮ÷³ĢČēĻĀĶ¼ĖłŹ¾”£


ŅŃÖŖ£ŗKSP(PbSO4)=1.82”Į10-8£¬KSP(PbCO3)=1.46”Į10-13Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³ö²½Öč¢Ł”°×Ŗ»Æ”±µÄĄė×Ó·½³ĢŹ½__________________”£
(2)øł¾ŻÓŅĶ¼Čܽā¶ČĒśĻß(g/100gĖ®)£¬ÓÉĀĖŅŗIµĆµ½Na2SO4¹ĢĢåµÄ²Ł×÷ĪŖ£ŗ½«”°ĀĖŅŗ1”±”¢_________”¢_________”¢ÓĆŅŅ“¼Ļ“µÓŗóøÉŌļ”£
(3)²½Öč¢Ū”°ĖįČÜ”±£¬ĪŖĢįøßĖįČÜĖŁĀŹ£¬æɲÉČ”µÄ“ėŹ©ŹĒ________________(ČĪŅāŠ“³öŅ»Ģõ)
(4)”°ĀĖŅŗ2”±ÖŠæÉŃ»·ĄūÓƵÄČÜÖŹĪŖ_______(Ģī»ÆѧŹ½)”£Čō²½Öč¢Ü”°³ĮĒ¦”±ŗóµÄĀĖŅŗÖŠc(Pb2+)=1.82”Į10-5 mol”¤L-1£¬Ōņ“ĖŹ±c(SO42-)=________mol”¤L-1”£
(5)²½Öč¢Ž”°ŗĻ³É”±ČżŃĪµÄ»Æѧ·½³ĢŹ½ĪŖ____________________”£
(6)ČōĻūŗÄ100.0tĒ¦Äą£¬×īÖÕµĆµ½“æ¾»øÉŌļµÄČżŃĪ49.5t£¬¼ŁÉčĒ¦ÄąÖŠµÄĒ¦ŌŖĖŲÓŠ75£„×Ŗ»ÆĪŖČżŃĪ£¬ŌņĒ¦ÄąÖŠĒ¦ŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ___________”£
”¾“š°ø”æPbSO4+CO32-=PbCO3+SO42- ÉżĪĀ½į¾§ ³ĆČČ¹żĀĖ ŹŹµ±ÉżĪĀ£ØŹŹµ±Ōö¼ÓĻõĖįÅØ¶Č£¬»ņ½«ĀĖŌü·Ū“āŌö“ó±ķĆ껿µČ£© HNO3 1”Į10-3 4PbSO4+6NaOH![]() 3PbOPbSO4H2O +3Na2SO4+2H2O 55.20%
3PbOPbSO4H2O +3Na2SO4+2H2O 55.20%
”¾½āĪö”æ
£Ø1£©ÓÉÓŚKSP(PbSO4)=1.82”Į10-8£¾KSP(PbCO3)=1.46”Į10-13£¬ĖłŅŌ²½Öč¢Ł¼ÓČėĢ¼ĖįÄĘČÜŅŗ£¬°ŃĮņĖįĒ¦×Ŗ»ÆĪŖĢ¼ĖįĒ¦£»
£Ø2£©½«”°ĀĖŅŗ1”±ÉżĪĀ½į¾§”¢³ĆČČ¹żĀĖ”¢ÓĆŅŅ“¼Ļ“µÓŗóøÉŌļµĆµ½Na2SO4¹ĢĢ壻
£Ø3£©ĪŖĢįøßĖįČÜĖŁĀŹ£¬æÉŹŹµ±ÉżĪĀ£¬»ņŹŹµ±Ōö¼ÓĻõĖįÅØ¶Č£¬»ņ½«ĀĖŌü·Ū“āŌö“ó±ķĆ껿µČ£»
£Ø4£©Pb”¢PbOŗĶPbCO3ŌŚĻõĖįµÄ×÷ÓĆĻĀ×Ŗ»Æ³ÉPb£ØNO3£©2£¬Pb£ØNO3£©2ÖŠ¼ÓĻ”H2SO4×Ŗ»Æ³ÉPbSO4ŗĶĻõĖį£¬HNO3æÉŃ»·ĄūÓĆ£¬øł¾ŻKSP(PbSO4)=1.82”Į10-8£¬ČōĀĖŅŗÖŠc£ØPb2+£©=1.82”Į10-5mol/L£¬ŌņČÜŅŗÖŠµÄc(SO42-)= KSP(PbSO4)/c£ØPb2+£©=1.82”Į10-8/1.82”Į10-5=1”Į10-3mol/L£»
£Ø5£©”°ŗĻ³É”±ČżŃĪµÄ»Æѧ·½³ĢŹ½ĪŖ4PbSO4+6NaOH![]() 3PbOPbSO4H2O+3Na2SO4+2H2O£»
3PbOPbSO4H2O+3Na2SO4+2H2O£»
£Ø6£©øł¾ŻĒ¦ŌŖĖŲŹŲŗć¼ĘĖćĒ¦ÄąÖŠĒ¦ŌŖĖŲµÄÖŹĮæ·ÖŹż”£
£Ø1£©ÓÉÓŚKSP(PbSO4)=1.82”Į10-8£¾KSP(PbCO3)=1.46”Į10-13£¬ĖłŅŌ²½Öč¢Ł¼ÓČėĢ¼ĖįÄĘČÜŅŗ£¬°ŃĮņĖįĒ¦×Ŗ»ÆĪŖĢ¼ĖįĒ¦£¬ŅŌĢįøßŌĮĻµÄĄūÓĆĀŹ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖPbSO4+Na2CO3=PbCO3+Na2SO4£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗPbSO4+CO32-=PbCO3+SO42-£¬
¹Ź“š°øĪŖ£ŗPbSO4+CO32-=PbCO3+SO42-”£
£Ø2£©ĀĖŅŗ¢ńµÄČÜÖŹÖ÷ŅŖŹĒNa2SO4ŗĶ¹żĮæµÄNa2CO3£¬½«”°ĀĖŅŗ1”±ÉżĪĀ½į¾§”¢³ĆČČ¹żĀĖ”¢ÓĆŅŅ“¼Ļ“µÓŗóøÉŌļµĆµ½Na2SO4¹ĢĢ壬
¹Ź“š°øĪŖ£ŗÉżĪĀ½į¾§”¢³ĆČČ¹żĀĖ”£
£Ø3£©ĪŖĢįøßĖįČÜĖŁĀŹ£¬æÉŹŹµ±ÉżĪĀ£¬»ņŹŹµ±Ōö¼ÓĻõĖįÅØ¶Č£¬»ņ½«ĀĖŌü·Ū“āŌö“ó±ķĆ껿µČ£¬
¹Ź“š°øĪŖ£ŗŹŹµ±ÉżĪĀ£ØŹŹµ±Ōö¼ÓĻõĖįÅØ¶Č£¬»ņ½«ĀĖŌü·Ū“āŌö“ó±ķĆ껿µČ£©”£
£Ø4£©Pb”¢PbOŗĶPbCO3ŌŚĻõĖįµÄ×÷ÓĆĻĀ×Ŗ»Æ³ÉPb£ØNO3£©2£¬Pb£ØNO3£©2ÖŠ¼ÓĻ”H2SO4×Ŗ»Æ³ÉPbSO4ŗĶĻõĖį£¬HNO3æÉŃ»·ĄūÓĆ£¬øł¾ŻKSP(PbSO4)=1.82”Į10-8£¬ČōĀĖŅŗÖŠc£ØPb2+£©=1.82”Į10-5mol/L£¬ŌņČÜŅŗÖŠµÄc(SO42-)= KSP(PbSO4)/c£ØPb2+£©=1.82”Į10-8/1.82”Į10-5=1”Į10-3mol/L£¬
¹Ź“š°øĪŖ£ŗHNO3£¬1”Į10-3”£
£Ø5£©øł¾ŻĢāÄ抚Źö£¬½įŗĻ×Ŗ»Æ¹ŲĻµ£¬Ōņ²½Öč¢Ž”°ŗĻ³É”±ČżŃĪµÄ»Æѧ·½³ĢŹ½ĪŖ4PbSO4+6NaOH![]() 3PbOPbSO4H2O+3Na2SO4+2H2O£¬
3PbOPbSO4H2O+3Na2SO4+2H2O£¬
¹Ź“š°øĪŖ£ŗ4PbSO4+6NaOH![]() 3PbOPbSO4H2O +3Na2SO4+2H2O”£
3PbOPbSO4H2O +3Na2SO4+2H2Oӣ
£Ø6£©ÉčĒ¦ÄąÖŠĒ¦ŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖx£¬øł¾ŻĒ¦ŌŖĖŲŹŲŗćæÉµĆ£ŗ
100.0”Į106g”Įx”Į75%/207g/mol=49.5”Į106g/990g/mol”Į4£¬½āµĆx=0.5520£¬ĖłŅŌĒ¦ÄąÖŠĒ¦ŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ55.20%£¬¹Ź“š°øĪŖ£ŗ55.20%”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹÆÄ«Ļ©ŹĒÄæĒ°æĘ¼¼ŃŠ¾æµÄČČµć£¬æÉæ“×÷½«ŹÆÄ«µÄ²ćד½į¹¹Ņ»²ćŅ»²ćµÄ°žæŖµĆµ½µÄµ„²ćĢ¼Ō×Ó”£½«ĒāĘų¼ÓČėµ½ŹÆÄ«Ļ©ÅÅĮŠµÄĮł½Ē¾§øńÖŠæɵĆ×ī±”µÄµ¼µē²ÄĮĻŹÆÄ«Ķé(ČēĻĀĶ¼)£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ

A. ŹÆÄ«Ļ©ÓėŹÆÄ«Ķ黄ĪŖĶ¬ĻµĪļ
B. ŹÆÄ«Ļ©×Ŗ±äĪŖŹÆÄ«ĶéæÉæ“×÷Č”“ś·“Ó¦
C. ŹÆÄ«Ļ©ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕ£¬Ö»²śÉś¶žŃõ»ÆĢ¼ĘųĢ唣
D. ŹÆÄ«ĶéµÄ»ÆѧŹ½ĶØŹ½ŹĒCnH2n+2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
A. 10g46%¼×Ėį(HCOOH)Ė®ČÜŅŗĖłŗ¬µÄŃõŌ×ÓŹżĪŖ0.5NA
B. 1molCnH2n+2Ėłŗ¬µÄ¹²ÓƵē×Ó¶ŌŹżĪŖ(2n+1)NA
C. ŗ¬ÓŠC©SiŹżÄæĪŖ2NAµÄSiC¾§ĢåÖŠ¹čŌ×ÓµÄĪļÖŹµÄĮæĪŖ1mol
D. ³£ĪĀĻĀ£¬5.6gFeÓėŗ¬0.2molHNO3µÄČÜŅŗ³ä·Ö×÷ÓĆ£¬×īÉŁ»įŹ§Č„µē×ÓŹżĪŖ0.15NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃéĖłŃ”ŌńµÄŹŌ¼Į”¢×°ÖĆ»ņŅĒĘ÷(¼Š³Ö×°ÖĆŅŃĀŌ Č„)ÄÜ“ļµ½ĻąÓ¦ŹµŃéÄæµÄµÄŹĒ
A. ĢįČ”äåĖ®ÖŠµÄäå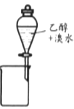
B. ŃéÖ¤ŹÆĄÆÓĶ·Ö½ā²śĪļÖŠŗ¬ÓŠĻ©Ģž
C. ŃéÖ¤H2O2 ·Ö½āŹ±¶žŃõ»ÆĆĢµÄ“߻Ɗ§¹ūÓÅÓŚĀČ»ÆĢś
D. ĮæČ”20.00mL 0.1000mol/L HClČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚĀČĖ®µÄŠšŹö£¬ÕżČ·µÄŹĒ
A. ŠĀÖĘĀČĖ®ÖŠÖ»ŗ¬Cl2ŗĶH2O·Ö×Ó
B. ŠĀÖĘĀČĖ®æÉŹ¹Ą¶É«ŹÆČļŹŌÖ½ĻȱäŗģŗóĶŹÉ«
C. ¹āÕÕĀČĖ®ÓŠĘųÅŻŅŻ³ö£¬øĆĘųĢåŹĒCl2
D. ĀČĖ®·ÅÖĆŹżĢģŗóĖįŠŌ¼õČõ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
A.14gµŖĘųŗ¬ÓŠNAøöµŖŌ×Ó
B.±ź×¼×“æöĻĀ£¬22.4L H2Oŗ¬ÓŠĒāŌ×ÓøöŹżĪŖ2NA
C.20gD2OÖŠĖłŗ¬µÄÖŹ×ÓŹżĪŖ10NA
D.25”ę”¢101kPaŹ±£¬ŗ¬NAøöĒā·Ö×ÓµÄĘųĢåѳʷĢå»ż“óÓŚ22.4L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ£ŃóÖ²ĪļČēŗ£“ųŗ£ŌåÖŠŗ¬ÓŠ·įø»µÄµāŌŖĖŲ£¬ŹµŃéŹŅĄļ“Óŗ£ŌåÖŠĢįČ”µāµÄĮ÷³ĢČēĶ¼£ŗ
 Ēė»Ų“š£ŗ
Ēė»Ų“š£ŗ
£Ø1£©Š“³öĢįČ”¹ż³ĢÖŠÓŠ¹ŲŹµŃé²Ł×÷µÄĆū³Ę£ŗ¢Ł____”¢¢Ū___”£
£Ø2£©²Ł×÷¢ŪÓƵ½µÄÖ÷ŅŖ²£Į§ŅĒĘ÷____”£
£Ø3£©ĢįČ”µāµÄ¹ż³ĢÖŠ£¬æɼÓČėµÄÓŠ»śČܼĮŹĒ___£¬ÓĆĮ¦Õńµ“”¢¾²ÖĆŗó£¬ÉĻ²ć³Ź___É«£¬ĻĀ²ć³Ź____É«”£
£Ø4£©Š“³ö¢ŚµÄĄė×Ó·½³ĢŹ½_____”£
£Ø5£©¹¤ŅµĢįČ”µĆµ½µÄµāæÉÓĆÓŚÖĘŅ©Ę·”Ŗ”Ŗ»ŖĖŲʬ£ØĪ÷µŲµāʬ£©£¬Ęä»īŠŌ³É·ÖĪŖ·Ö×Óµā”£ĒėÄćÉč¼ĘŅ»ÖÖ·½·ØĄ“ŃéÖ¤»ŖĖŲʬ֊µÄ·Ö×Óµā£¬Ęä·½·ØŹĒ£ØÓĆĪÄ×ÖĆčŹö£©£ŗ__”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ¢ŁÓŠ»ś»Æѧ·“Ó¦Ņņ·“Ó¦Ģõ¼ž²»Ķ¬£¬æÉÉś³É²»Ķ¬µÄÓŠ»ś²śĘ·”£ĄżČē£ŗ

¢Ś±½µÄĶ¬ĻµĪļÓėĀ±ĖŲµ„ÖŹ»ģŗĻ£¬ČōŌŚ¹āÕÕĢõ¼žĻĀ£¬²ąĮ“Ģž»łÉĻµÄĒāŌ×Ó±»Ā±ĖŲŌ×ÓČ”“ś£»ČōŌŚ“߻ƼĮ×÷ÓĆĻĀ£¬±½»·Ä³Š©Ī»ÖĆÉĻµÄĒāŌ×Ó±»Ā±ĖŲŌ×ÓČ”“ś”£¹¤ŅµÉĻ°“ĻĀĮŠĀ·ĻßŗĻ³É½į¹¹¼ņŹ½ĪŖ µÄĪļÖŹ£¬øĆĪļÖŹŹĒŅ»ÖÖĻćĮĻ”£
µÄĪļÖŹ£¬øĆĪļÖŹŹĒŅ»ÖÖĻćĮĻ”£

Ēėøł¾ŻÉĻŹöĀ·Ļߣ¬»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AµÄ½į¹¹¼ņŹ½æÉÄÜĪŖ______”£
£Ø2£©·“Ó¦¢ÜµÄ·“Ó¦Ģõ¼žĪŖ______£¬·“Ó¦¢ŻµÄĄąŠĶĪŖ______”£
£Ø3£©·“Ó¦¢ŽµÄ»Æѧ·½³ĢŹ½ĪŖ£ØÓŠ»śĪļŠ“½į¹¹¼ņŹ½£¬²¢×¢Ć÷·“Ó¦Ģõ¼ž£©£ŗ______”£
£Ø4£©¹¤ŅµÉś²śÖŠ£¬ÖŠ¼ä²śĪļAŠė¾·“Ó¦¢Ū¢Ü¢ŻµĆD£¬¶ų²»²ÉČ”½«AÖ±½Ó×Ŗ»ÆĪŖDµÄ·½·Ø£¬ĘäŌŅņŹĒ______”£
£Ø5£©ÕāÖÖĻćĮĻ¾ßÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬Ęä֊ijŠ©ĪļÖŹÓŠĻĀĮŠĢŲÕ÷£ŗ¢ŁĘäĖ®ČÜŅŗÓöFeCl3ČÜŅŗ²»³Ź×ĻÉ«£»¢Ś±½»·ÉĻµÄŅ»äå“śĪļÓŠĮ½ÖÖ£»¢Ū·Ö×ÓÖŠÓŠ5ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒā”£Š“³ö·ūŗĻÉĻŹöĢõ¼žµÄĪļÖŹæÉÄܵĽį¹¹¼ņŹ½£ØÖ»Š“Ņ»ÖÖ£©£ŗ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ£Ø £©
A. CaCO3µÄµēĄė·½³ĢŹ½£ŗCaCO3 ![]() Ca2+£«CO32£
Ca2+£«CO32£
B. H2SO3µÄµēĄė·½³ĢŹ½H2SO3![]() 2H£«£«SO32£
2H£«£«SO32£
C. CO32£µÄĖ®½ā·½³ĢŹ½£ŗCO32££«2H2O![]() H2CO3£«2OH£
H2CO3£«2OH£
D. HCO3£ŌŚĖ®ČÜŅŗÖŠµÄµēĄė·½³ĢŹ½£ŗHCO3££«H2O![]() H3O£«£«CO32£
H3O£«£«CO32£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com