

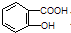
 ,同分异构体符合:①含有苯环; ②能发生银镜反应,不能发生水解反应,含有-CHO,不含酯基,③在稀NaOH溶液中,1mol该同分异构体能与2mol NaOH发生反应,则还含有2个-OH,④只能生成两种一氯代产物,则3个取代基相邻且-CHO处于2个羟基之间,或3个取代基处于间位;
,同分异构体符合:①含有苯环; ②能发生银镜反应,不能发生水解反应,含有-CHO,不含酯基,③在稀NaOH溶液中,1mol该同分异构体能与2mol NaOH发生反应,则还含有2个-OH,④只能生成两种一氯代产物,则3个取代基相邻且-CHO处于2个羟基之间,或3个取代基处于间位;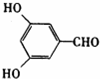 ,由关系图可知,B为
,由关系图可知,B为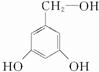 ,D为
,D为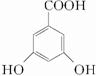 ,E为
,E为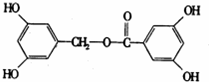 .
. ,
, ;
; ,含有的官能团为:酚羟基、酯基,故答案为:酚羟基、酯基;
,含有的官能团为:酚羟基、酯基,故答案为:酚羟基、酯基; +H2O
+H2O| 一定条件 |
 +
+ ,
, +H2O
+H2O| 一定条件 |
 +
+ ;
; ,同分异构体符合:①含有苯环; ②能发生银镜反应,不能发生水解反应,含有-CHO,不含酯基,③在稀NaOH溶液中,1mol该同分异构体能与2mol NaOH发生反应,则还含有2个-OH,④只能生成两种一氯代产物,则3个取代基相邻且-CHO处于2个羟基之间,或3个取代基处于间位,符合条件的同分异构体有如下两种:
,同分异构体符合:①含有苯环; ②能发生银镜反应,不能发生水解反应,含有-CHO,不含酯基,③在稀NaOH溶液中,1mol该同分异构体能与2mol NaOH发生反应,则还含有2个-OH,④只能生成两种一氯代产物,则3个取代基相邻且-CHO处于2个羟基之间,或3个取代基处于间位,符合条件的同分异构体有如下两种: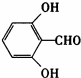 和
和 ,故答案为:2;
,故答案为:2; ,由关系图可知,B为
,由关系图可知,B为 ,D为
,D为 ,E为
,E为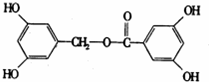 ,
, ,
, ;酯化.
;酯化.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在含有大量I-离子的溶液中:Cl-、Fe3+、Na+、Mg2+ |
| B、在由水电离出的c(H+)=10-12mol?L-1 的溶液中:Na+、Ba2+、Cl-、Br- |
| C、使甲基橙呈红色的溶液中:Fe2+、Na+、SO42-、ClO- |
| D、在加入Al能放出大量H2的溶液中:NH4+、SO42-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学课外活动小组应用如图所示的方法研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气,回答下列问题.
某化学课外活动小组应用如图所示的方法研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
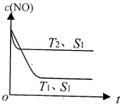 (1)汽车内燃机工作时发生反应:N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向5L密闭容器中充入6.5molN2和7.5molO2,在5min时反应达到平衡状态,此时容器中NO的物质的量是5mol.
(1)汽车内燃机工作时发生反应:N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向5L密闭容器中充入6.5molN2和7.5molO2,在5min时反应达到平衡状态,此时容器中NO的物质的量是5mol.查看答案和解析>>
科目:高中化学 来源: 题型:
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70℃ | 57.6℃ |
| TiCl4 | -25℃ | 136℃ |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=5.3的NaHSO3溶液:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3) |
| B、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、0.1mol?L-1 Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+2 c(H2CO3) |
| D、物质的量浓度相等的NH3?H2O和NH4Cl溶液等体积混合:c(Cl-)=c(NH3?H2O)+c(NH4+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com