
| 阳离子 | Ag+、Mg2+、Al3+、Ba2+ | ||
| 阴离子 | Cl-、SO
|
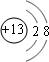
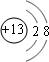
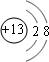 ;故答案为:离子键;极性共价键;
;故答案为:离子键;极性共价键;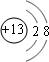


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | 乙 | 丙 | 丁 |
化合物中各元素原子个数比 | A∶C | B∶A | D∶E | B∶E |
1∶1 | 1∶2 | 1∶3 | 1∶4 |
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和,B原子最外层电子数比其次外层电子数多2个。在周期表中,C是E的邻族元素,化学性质活泼,D和E则位于同一周期,D和E的原子序数之和为30。
(1)写出元素符号:A___________,B___________,C___________,D___________,E___________。
(2)向甲的水溶液中加入MnO2,反应的化学方程式是____________________________。
(3)已知乙的式量小于甲,在实验室中常用什么方法制得乙:______________________
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会迅速产生大量气体和难溶物,有关离子方程式为______________________。
(5)向3 mL 1 mol·L-1KI溶液中依次注入下列试剂:①1 mL 5 mol·L-1盐酸;②0.5 mL 30%甲溶液;③1 mL丁。经充分振荡后静置,可得到紫色溶液,这种紫色溶液是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(9分)A、B、C、D、E五种短周期元素,已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的不同周期邻族元素;D和E的原子序数之和为30。它们两两形成的化合物为甲、乙、丙、丁四种。这四种化合物中原子个数比如下表:(用元素符号作答)
|
| 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
(1)写出A~E的元素符号
A: B: C: D: E:
(2)向甲的水溶液中加入MnO2,氧化产物是 。
(3)已知有机物乙的分子为平面结构,碳氢键键角为120°,实验室制取乙的化学方程式为:
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式是:
查看答案和解析>>
科目:高中化学 来源:2014届湖南省名校高三第一次大联考化学试卷(解析版) 题型:填空题
甲、乙、丙、丁四种物质之间具有如右转化关系:
请回答下列问题:
(1)若乙为两性不溶物,则丙转化为乙的离子方程式为 ;
(2)若丙为形成酸雨的主要物质,则甲的化学式 ,乙能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式为:
;
(3)若丙中含有目前人类使用最广泛的金属元素,且乙转化成丙为化合反应,则将丙溶液蒸发、灼烧得到的物质是 ,除去丙溶液中少量乙的方法是: (用化学方程式表示),如何检验乙溶液中的丙,请设计实验方案 。
查看答案和解析>>
科目:高中化学 来源:2014届浙江省温州市十校联合体高三上学期期初联考化学试卷(解析版) 题型:推断题
甲、乙、丙、丁四种物质之间具有如右转化关系: 。
。
请回答下列问题:
(1)若乙为两性不溶物,则丙转化为乙的离子方程式为 ;
(2)若丙为形成酸雨的主要物质,则甲的化学式 ,乙能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式为 ;
(3)若丙中含有目前人类使用最广泛的金属元素,且乙转化成丙为化合反应,则将丙溶液蒸发、灼烧得到的物质是 ,除去丙溶液中少量乙的方法是 (用化学方程式表示),如何检验乙溶液中的丙,请设计实验方案 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com